Физическая химия полимерных гелей Лекция 25 КИНЕТИКА НАБУХАНИЯ АКРИЛОВОГО И МЕТАКРИЛОВОГО ИОНИТОВ

Физическая химия полимерных гелей Лекция 24 СВОЙСТВА КИНЕТИЧЕСКИХ КОЭФФИЦИЕНТОВ МОДЕЛИ. ВЛИЯНИЕ ВЯЗКОСТИ РАСТВОРА И КОЛИЧЕСТВА НЕКОВАЛЕНТНЫХ СВЯЗЕЙ НА КИНЕТИКУ НАБУХАНИЯ ПОЛИМЕРОВ
19.12.2015Физическая химия полимерных гелей Лекция 29 ПОЛИМЕРНО-ЭКСТРАКЦИОННЫЙ МЕТОД РАЗДЕЛЕНИЯ РАСТВОРЕННЫХ ВЕЩЕСТВ.
20.12.2015Физическая химия полимерных гелей Лекция 25 КИНЕТИКА НАБУХАНИЯ АКРИЛОВОГО И МЕТАКРИЛОВОГО ИОНИТОВ
Физическая химия полимерных гелей
Ферапонтов Н. Б., Гагарин А. Н., Струсовская Н. Л., Токмачёв М. Г., Тробов Х.Т., Рубин Ф.Ф.
Москва, МГУ имени М. В. Ломоносова 2015 г.
В работе [1] показано, как ионная форма акрилового и метакрилового типов ионитов и концентрация равновесного раствора влияют на упруго– пластические свойства геля, и как это отражается на кинетике набухания ПГ.
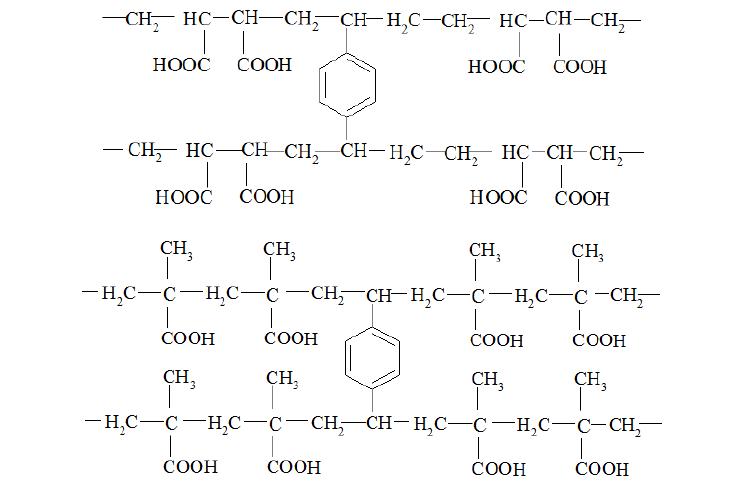
Строение ионообменников на основе полиакриловой (а), и полиметакриловой (б) кислот приведено на рис.1.
Рис. 1. Строение полиакриловой и полиметакриловой кислот [2].
Установлено, что в растворах хлорида натрия и в разбавленном растворе хлорида кальция гели проявляют упругие свойства, тогда как в концентрированном растворе хлорида кальция и в растворах хлорида никеля при деформации проявляется пластичность. Кроме того, было показано, что механизмы взаимодействия катионов Ca2+ и Ni2+ с атомами кислорода карбоксильных групп существенно различаются. Дело в том, что в водных растворах противоионы разного заряда и природы по разному связывают цепи полимеров на основе полиакрилатов (ПА) и полиметакрилатов (ПМА). В результате в полимерах возможны варианты связей, как с образованием ионных пар, так и с более сложными координационными соединениями, образующими дополнительные нековалентные сшивки между полимерными цепями.
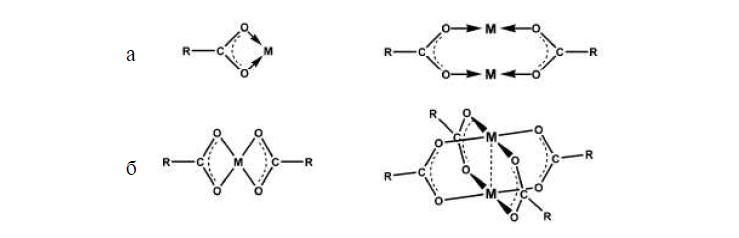
Кроме природы иона, на характер взаимодействия полимера с внешней средой достаточно сильно могут влиять концентрация раствора, температура и другие условия, что в свою очередь определяет конформационное состояние полимера и степень его набухания в растворе. Методом ИК спектроскопии для данных полимеров было установлено, что ионы двухвалентных переходных металлов (на примере Cu2+) и ионы трехвалентных металлов (Al3+) могут образовывать оба типа комплексов, как моно– так и биядерные (рис. 2). А ионы щелочноземельных металлов (Ca2+) могут образовывать только моноядерные комплексы, которые являются менее прочными, чем биядерные. Очевидно, что такая поливариантность будет оказывать влияние и на кинетику набухания полимера [3,4].
Рис.2. Структура моноядерного (а) и биядерного (б) комплексов металлов с карбоксильными группами [3].
Как было отмечено в [1], при проведении многократного нагревания и охлаждения системы ионит – раствор важную роль играет не только то, насколько сильно изменяется набухание ПГ с температурой, но и какова кинетика поглощения и выделения из него растворителя. Так как для осуществления разделительного процесса необходимо, чтобы скорости набухания и сжатия ионитов при изменении температуры были достаточно высокими, этому вопросу уделено особое внимание.
а б На рис. 3 и 4 представлены результаты исследования кинетики набухания некоторых ионитов в воде, полученные при изучении влияния температуры на процесс набухания. Они свидетельствуют о том, что кинетика даже близких по типу ионитов может различаться достаточно сильно.
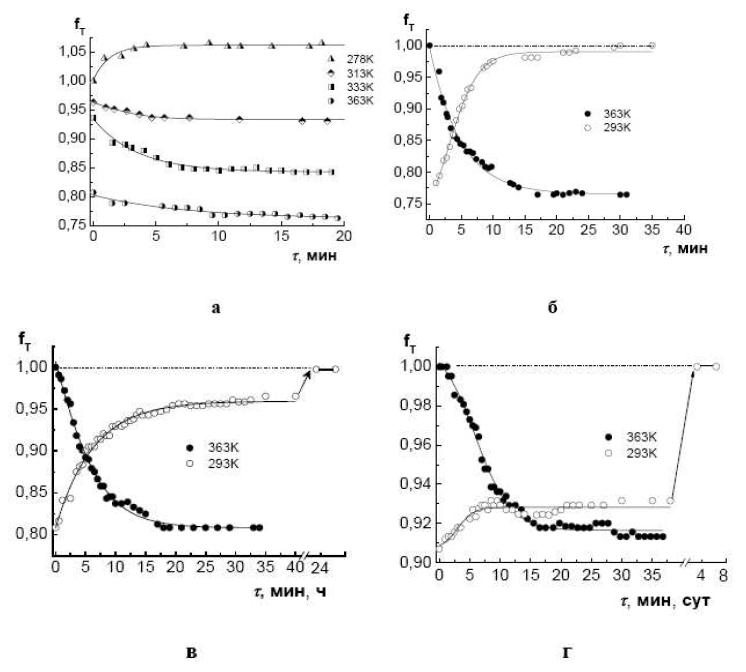
Скорости сжатия ионита КБ-4П2 в Ca2+–форме (после повышения температуры) и набухания (после ее понижения) достаточно высокие, так что исходный объем ионита успевает быстро восстановиться после нагревания и последующего охлаждения. Равновесные объемы устанавливаются в течение 10–20 мин как в случаях небольшого ~ 5K, так и в случае большого ~ 90K изменения температуры (рис. 3 а, б). Аналогично ведет себя ионит в Mg2+– форме в разбавленных растворах, однако, при концентрации раствора MgCl2 выше 2 г-экв/л скорость набухания при охлаждении значительно снижается (рис. 3 в). Равновесные объемы устанавливаются лишь в течение суток. Для Ni2+–формы даже при низких концентрациях внешнего раствора набухание протекает значительно медленнее, чем сжатие (рис. 3 г).
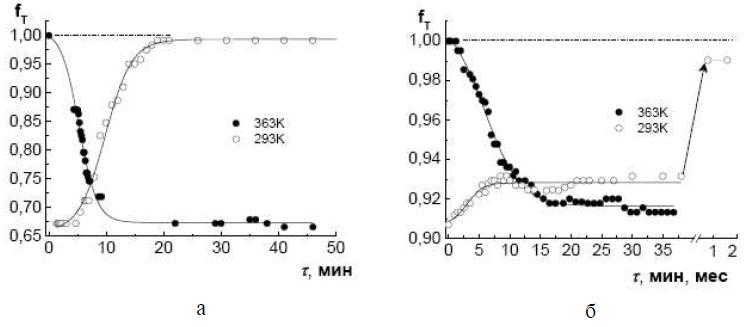
Для слабосшитого геля ПА/ПМА = 0.5 в Са2+– форме скорости сжатия полимера в результате нагревания и набухания в результате охлаждения очень высокие, однако, и в этом случае процесс набухания протекает медленнее, чем сжатие, и даже наблюдается плато на начальном участке кинетической кривой набухания (рис. 4 а). Для другого катионита КБ-2э3 в Са2+– форме сжатие гранулы после нагревания протекает очень быстро, однако, последующее набухание после охлаждения протекает чрезвычайно медленно. Равновесная степень набухания Са2+–формы катионита КБ-2э3 после охлаждения гранулы ионита не достигается даже через 2 месяца. За это время гранула увеличивает свой объем всего на ~ 6% (рис. 4 б). Автор предполагает, что, будучи однажды нагретой на 70K, данная система при охлаждении выходит на новое стационарное состояние набухания.
Рис. 3. Кинетика изменения относительного объема ионита КБ-4П2 после изменения температуры от 278 K до 363 K (а) и в Са– (б), Mg–(в), Ni– (г) формах после изменения температуры от 293 K до 363 K (темные точки) и от 363 K до 293 K (светлые точки).
Рис. 4. Изменение температурного коэффициента набухания слабосшитого геля ПА/ПМА=0.5 (а) и ионита КБ-2э3 (б) в Са2+–форме в 2.5 н СaCl2 во времени после изменения температуры от 293 K до 363 K (темные точки) и от 363 K до 293 K (светлые точки).
а б Попытка установить причины такого поведения полимеров данного типа была сделана в другой серии опытов. На рис. 5 представлены изображения, полученные через определенные промежутки времени после того, как сухая гранула ионита КБ-4П2 в Na+– форме была помещена в 1 н раствор NiCl2. Видно, что на начальном этапе внутри гранулы существует контрастная резкая граница между сухим центром и внешней набухшей оболочкой. В некоторый, очень близкий к начальному, момент времени сухой центр выглядит как светлый центральный кружок, а набухшая оболочка, как темный круг, обрамляющий центр гранулы. Светлая зона за пределами внешней оболочки гранулы – внешний раствор, попавший в поле видимости окуляра. Постепенно контрастная граница движется к центру гранулы, сухая зона уменьшается до тех пор, пока не исчезает полностью.
Рис. 5. Фотографии зерна ионита КБ-4П2, показывающие изменение во времени площади сухой зоны и набухшей оболочки после помещения сухой гранулы в 1 н раствор NiCl2.
Существование подобной резкой контрастной границы между сухим или сколлапсированным ядром геля и набухшей оболочкой ранее наблюдали даже в случае слабосшитого гидрофильного полимера (ССГП) без ионообменных групп [5]. В работе в таком процессе выделили три этапа:
1. После того, как сухой сколлапсированный гель поместили в «хороший» растворитель, вначале наблюдался инкубационный период, в течение которого гель продолжал оставаться в сколлапсированном состоянии.
2. Затем имел место период сосуществования двух фаз: на поверхности геля появлялся тонкий слой набухшей фазы и со временем слой набухшей фазы рос. При этом к центру гранулы двигалась резкая граница между набухшей и сколлапсированной фазами. В некоторый момент времени граница раздела двух фаз достигала центра и исчезала.
3. После этого наступал период набухания одной фазы, так как после того, как сколлапсированная фаза исчезала, гранула еще не достигала равновесного объема и продолжала набухать.
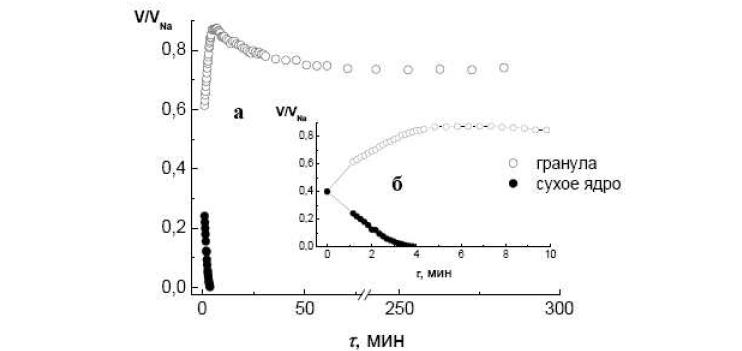
Сжатие того же геля после того, как его вновь помещали в «плохой» растворитель, протекало в такие же три этапа, что и набухание. При этом максимальное изменение объема геля при набухании происходит не на 3–ем этапе, а в случае перехода в сколлапсированное состояние на 2–ой стадии, в период сосуществования двух фаз. В рассматриваемом случае параллельно и с разными скоростями протекают два процесса: набухания Na+–формы и сжатия набухшего слоя (полностью или частично) при замене иона Na+ на ион Ni2+. Кинетические изменения объемов гранулы ионита и сухого ядра в таких опытах представлены на рис. 6. Сначала общий объем гранулы увеличивается, а затем вновь уменьшается, достигая стационарного значения. Первоначально резкое увеличение объема гранулы вызвано быстрой диффузией воды в Na+– форму ионита, а последующее сжатие – в результате более медленной реакции обмена ионов Na+ на Ni2+. Это приводит к тому, что образуется и постепенно продвигается к центру более плотная зона никелевой формы (граница между никелевой и натриевой формами на фотографиях не различима).
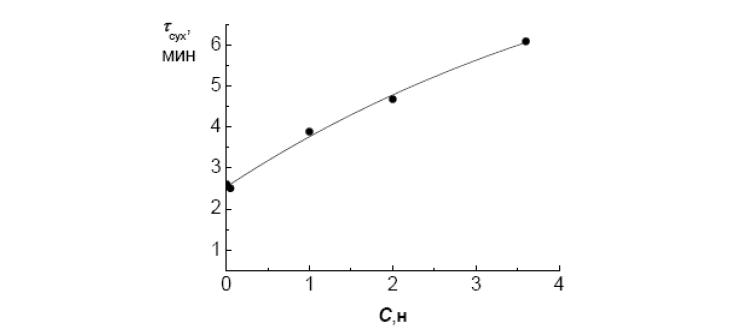
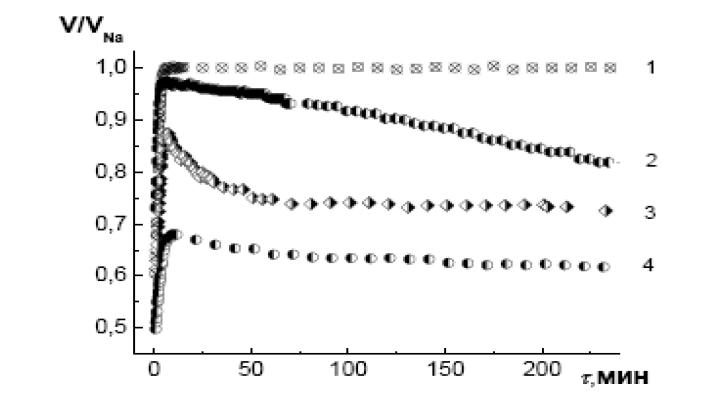
Нельзя не обратить внимание на тот факт, что набухание гранулы и исчезновение сухого центра завершается в считанные минуты, хотя известно, что ионный обмен с заменой системы ионных связей карбоксилат–натрий на систему координационных связей никеля с несколькими карбоксилатными лигандами длится не менее часа. Автор [1] утверждает, что этот процесс неизбежно связан с приближением нескольких функциональных групп полимерной сетки к комплексообразующему иону металла, медленным перестроением конформации соответствующих сегментов полимерных цепей и уменьшением объема набухшей гранулы. С увеличением концентрации раствора хлорида никеля скорость движения границы между набухшей оболочкой и сухим центром уменьшается (рис. 7). Одновременно замедляется и приближение к равновесному (вернее, стационарному) объему зерна в целом (рис. 8). Это подтверждает роль внешней оболочки Ni2+– формы, которая с концентрацией раствора становится более плотной, что затрудняет диффузионный перенос воды и ионов через нее, но в еще большей степени замедляет конформационное перестроение структуры полимерной сетки из Na+ в Ni2+-форму.
Рис. 6. Кинетические кривые изменения объема гранулы ионита КБ-4П2 и сухого ядра в 1 н растворе NiCl2. На рис. 6 б показан начальный участок зависимости.
Рис. 7. Зависимость времени исчезновения сухого ядра от концентрации раствора хлорида никеля.
Рис. 8. Кинетические кривые изменения коэффициента набухания сухих гранул ионита КБ-4П2 в Nа+–форме от времени, помещенных в дистиллированную воду (1), в раствор хлорида никеля с концентрацией: 0,005 н (2), 1 н (3), 4 н (4).
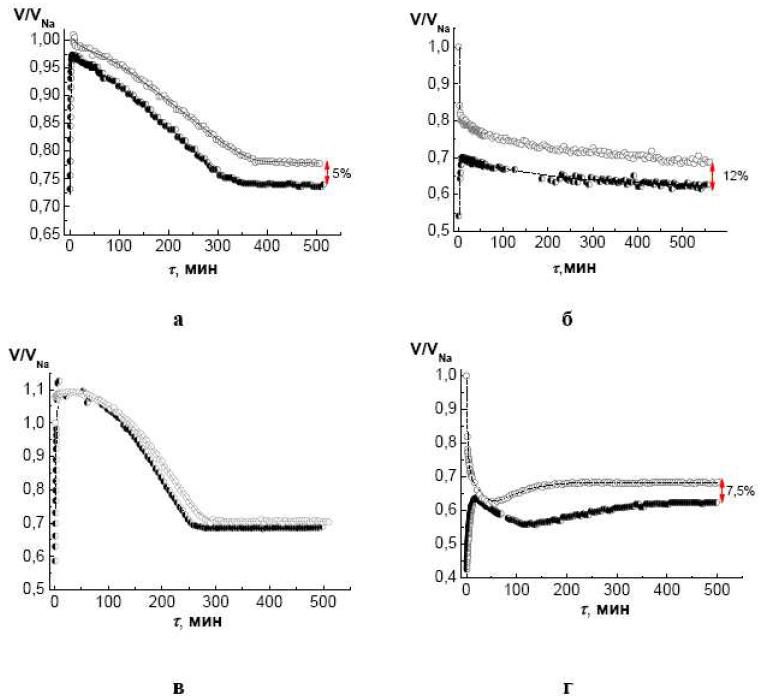
«Жесткость» (малую «эластичность») внешней оболочки гранулы ионита в форме иона никеля подтвердили в следующих опытах. На рис. 9 (а) и (б) сопоставлены пары кинетических кривых в опытах, в которых в растворы хлоридов никеля и кальция помещали одну и ту же гранулу ионита КБ-4П2 в Na+–форме в сухом (темные точки) и в набухшем в воде (светлые точки) состояниях. Оказалось, что конечные стационарные объёмы одной и той же гранулы в растворе хлорида никеля не совпадают: сухая гранула, помещенная в раствор хлорида никеля, не достигает того предельно набухшего состояния, которое устанавливается для изначально набухшей гранулы. Различие в объемах увеличивается с ростом концентрации внешнего раствора.
Рис. 9. Кинетические кривые в опытах, в которых в растворы хлоридов никеля (а) и (б) и кальция (в) и (г) с концентрациями 0.005 н (а) и (в) и 4 н (б) и (г) помещали одну и ту же гранулу ионита КБ-4П2 в Na+– форме в сухом (темные точки) и в набухшем в воде (светлые точки) состояниях.
Действительно, на различии в объемах одной и той же гранулы ионита, полученной из двух разных исходных состояний, не может не сказаться то обстоятельство, что процесс замены ионов Na+ на ионы Ni2+ в изначально сухой грануле происходит при значительно меньшей степени гидратации полимерных цепей. В этом случае сближенными для образования достаточно прочных бис–карбоксилатных комплексов с ионами Ni2+ оказываются иные наборы карбоксильных групп, чем это имеет место при ионном обмене на Ni2+ в предварительно набухшей грануле. Здесь наблюдается прямая аналогия с тем фактом, что при химическом сшивании полимерных цепей в растворе бифункциональными реагентами способность к набуханию у конечных гелей быстро уменьшается с ростом концентрации исходного раствора полимера [6].
Данные на рис. 9 в, показывают, что стационарные значения коэффициента набухания гранулы ионита КБ-4П2 из двух исходных состояний в разбавленном растворе хлорида кальция практически совпадают, то есть в обоих случаях медленно достигаются близкие к равновесным состояния сорбции воды и ионов кальция. Для концентрированного раствора (рис.8) наблюдается несколько другая картина. Объём сухой гранулы, помещенной в раствор хлорида кальция, сначала увеличивается за счет быстрой сорбции воды, потом уменьшается в результате протекания реакции ионного обмена, а затем гранула продолжает набухать, достигая конечного стационарного состояния. В этот период, вероятно, происходит перестраивание системы электростатических связей двухзарядного иона кальция с карбоксильными анионами. Соединения карбоксильных групп с кальцием носят скорее ионный, чем координационный характер. Они намного более лабильны, чем комплексы никеля, и быстро обменивают карбоксилатные лиганды, позволяя связанным с ними полимерным цепям изменять свое конформационное состояние и постепенно снижать локальные напряжения всей полимерной сетки.
Поведение ионообменных систем, о которых шла речь выше, могут осложнять сопутствующие реакции образования малорастворимых соединений и комплексных соединений различного строения. В частности, в данной системе из-за гидролиза соли в слабощелочной среде внутри исходной гранулы (натриевая форма ионита) можно предположить образование фазы гидроксида никеля.
ЛИТЕРАТУРА.
1. Титова О.И. Безреагентное концентрирование и очистка растворов электролитов на термочувствительных сшитых полиэлектролитах. // Дисс. канд. хим. наук. – М., МГУ, 2013, 142с.
2. Салдадзе К.М., Пашков А.Б., Титов В.С. Ионообменные высокомолекулярные соединения. М.: Госхимиздат. 1960. 356 с.
3. Konradi R., R he J. Interaction of poly(methacrylic acid) brushes with metalions: an infrared investigation. // Macromolecules. 2004. V. 37. No 18. P. 6954–6961.
4. Konradi R., R he J. Interaction of Poly(methacrylic acid) Brushes with Metal Ions: Swelling Properties. // Macromolecules. 2005. V. 38. No 10. P. 4345– 4354.
5. Tomari T., Doi M. Hysteresis and incubation in the dynamics of volume transition of spherical gels. // Macromolecules. 1995. V. 28. P. 8334-8343.
6. Davankov V.A., Rogozhin S.V., Tsyurupa M.P. Factors determining theswelling power of crosslinked polymers. // Angew. Makromol. Chem. 1973.V. 32 P. 145-151.