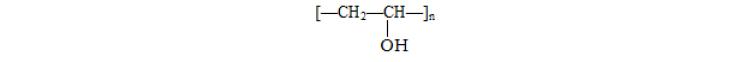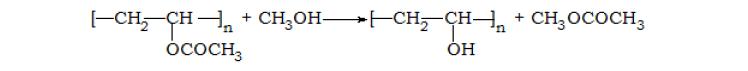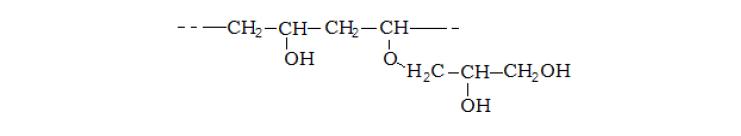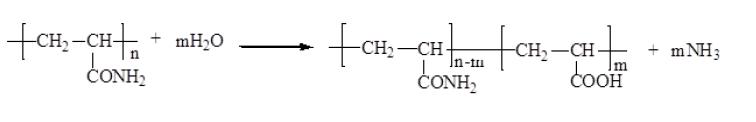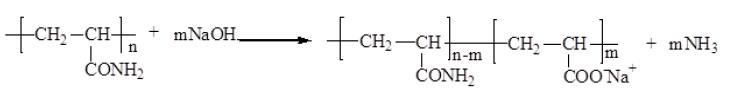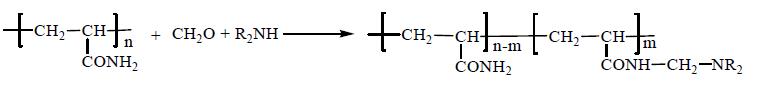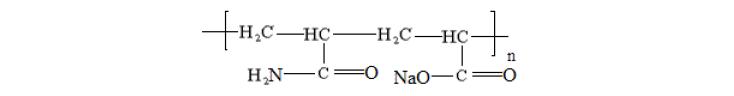Физическая химия полимерных гелей Лекция 3 СШИТЫЕ ГИДРОФИЛЬНЫЕ ПОЛИМЕРЫ С НЕДИССОЦИИРУЮЩИМИ ПОЛЯРНЫМИ ГРУППАМИ.

Физическая химия полимерных гелей Лекция 2 ГИДРОФИЛЬНЫЕ ПОЛИМЕРЫ. СШИТЫЕ ПОЛИЭЛЕКТРОЛИТЫ. ПОЛУЧЕНИЕ И СТРОЕНИЕ
25.11.2015
Физическая химия полимерных гелей Лекция 4 ЧТО ТАКОЕ ГЕЛИ ГИДРОФИЛЬНЫХ ПОЛИМЕРОВ?
27.11.2015Физическая химия полимерных гелей Лекция 3 СШИТЫЕ ГИДРОФИЛЬНЫЕ ПОЛИМЕРЫ С НЕДИССОЦИИРУЮЩИМИ ПОЛЯРНЫМИ ГРУППАМИ.
Физическая химия полимерных гелей
Ферапонтов Н. Б., Гагарин А. Н., Струсовская Н. Л., Токмачёв М. Г., Тробов Х.Т., Рубин Ф.Ф.
Москва, МГУ имени М. В. Ломоносова 2015 г.
1. Получение поливинилового спирта.
Поливиниловый спирт (ПВС) – полимер общей формулы:
Поскольку большинство гидроксильных групп ПВС связаны между собой водородными связями, ПВС растворяется лишь в горячей воде (80 – 100°С) при перемешивании в течение 2 – 4 часов. Водные растворы ПВС нестабильны при хранении: через несколько часов после приготовления начинается гелеобразование [1].
ПВС производится в больших количествах и широко применяется в различных областях. Например, для консервирования донорской кожи, изготовления печатных плат и клише в полиграфической промышленности, для получения поливинилацеталей, а также для приготовления лекарственного препарата «йодинол».
ПВС нельзя синтезировать напрямую полимеризацией винилового спирта, так как последний, в момент получения, изомеризуется в ацетальдегид или окись этилена. Наиболее распространенный способ получения ПВС – гидролиз или алкоголиз полимеров сложных виниловых эфиров [2, с.323 – 325]. В промышленности ПВС получают алкоголизом, в основном метанолизом, поливинилацетата (в качестве катализатора – кислота или щелочь):
Рис. 1. Схема получения ПВС метанолизом.
В полученном ПВС обычно содержатся остаточные О-ацетильные группы, количество которых в зависимости от условий процесса может изменяться от 0,05 до 5,00 % по массе.
В зависимости от катализатора, использованного при омылении поливинилацетата, ПВС может содержать различные трудноудаляемые примеси [2, с.788–792]. ПВС, полученный при омылении в присутствии щелочи, содержит ацетат натрия, приводящий к окрашиванию полимера при прогреве. При алкоголизе поливинилацетата в присутствии серной, соляной или хлорной кислот получают ПВС без примеси солей. Однако, при применении серной кислоты некоторая часть гидроксильных групп ПВС взаимодействует с ней с образованием сернокислых эфиров, которые могут отщеплять Н2SO4, способствующую деструкции полимера. При применении соляной кислоты образуется ПВС, окрашенный в светло-желтый цвет.
2. Применение агентов, образующих поперечные связи Использование эпихлоргидрина.
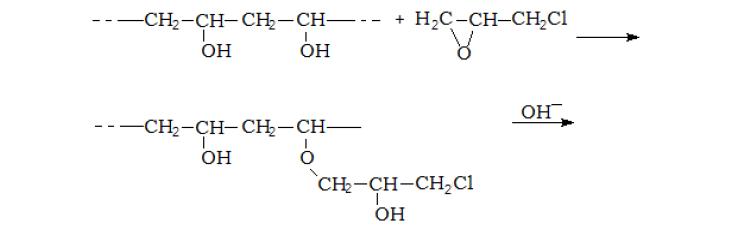
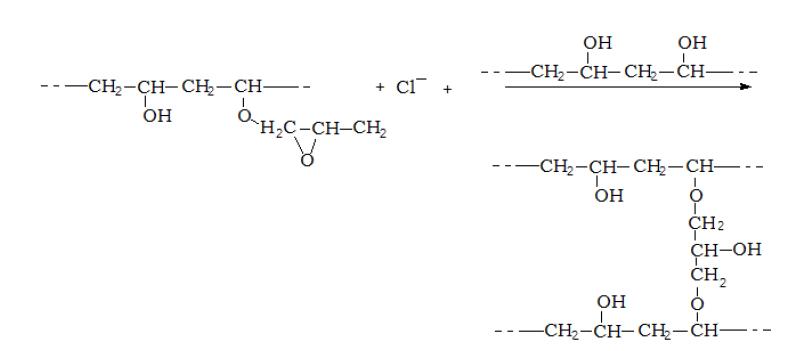
В щелочной среде ковалентно–сшитые гели ПВС можно получать с помощью эпихлоргидрина (ЭХГ) [3-5] согласно следующей схеме:
Рис.2. Схема получения ПВС, сшитого ЭХГ.
Естественно, в этом случае можно ожидать побочных реакций, приводящих, например, лишь к модифицированному глицерином полимеру.
Однако у полученного таким образом сшитого ПВС есть важное преимущество: он механически прочен и химически устойчив к действию кислот и щелочей.
3. Использование диальдегидов.
Наиболее изученными являются гели ПВС, сшитого диальдегидами.
Они широко используются при получении различного рода хроматографических материалов и мембран. В литературе описано использование глутарового [6], янтарного [7] диальдегидов, терефталевого [8, 9] тиодиацетальальдегида [10, 11] для получения химически сшитых гелей ПВС. При этом одна альдегидная группа диальдегида реагирует с двумя гидроксильными группами, входящими в состав одной цепи ПВС, а другая альдегидная группа связывается с соседней макромолекулой.
Необходимым условием сшивания ПВС диальдегидами является кислая реакция среды. Эффективность процесса сшивания макромолекул ПВС в водном растворе глутаровым альдегидом повышается при увеличении концентрации полимера в исходном растворе и увеличении концентрации сшивающего агента (при одинаковой концентрации полимера).
Использование полимера большей молекулярной массы тоже способствует увеличению эффективности сшивания. Присутствие в полимере большого числа О-ацетильных групп (до 30%) снижало эффективность сшивания в 1,3–1,4 раза [12].
Также в качестве сшивающих агентов могут использоваться янтарная, малеиновая, полиакриловая кислоты и п-ксилендихлорид [13].
4. Гели ПВС с борной кислотой и боратами.
ПВС весьма чувствителен к следам соединений бора, особенно борной кислоты, буры и перборатов. Гелеобразование имеет место в растворах, содержащих не менее 2% полимера и не менее 1% борной кислоты или буры.
Эти комплексы, по-видимому, не представляют собой определенного продукта и образуются путем соединения линейных цепей ПВС поперечными связями вследствие комплексообразования. Они представляют собой вязкие неэластичные аморфные системы, однако, при кратковремен- ном приложении нагрузки они ведут себя как упругие тела. Плавление происходит при невысоких температурах порядка 30 – 40°С. Механические свойства, и в частности модуль упругости, возрастает при увеличении молекулярной массы и уменьшении содержания остаточных О-ацетильных групп, увеличении концентрации полимера и буры. Также отмечалось снижение модуля упругости гелей при повышении температуры [14].
5. Гели ПВС с медно-аммиачным раствором.
Водный медно-аммиачный раствор придает нерастворимость ПВС. В этом отношении он отличается от других аналогичных соединений, потому что комплексные аммиачные соединения, содержащие цинк, никель, серебро не оказывают никакого действия на снижение водорастворимости. Связи между цепями относятся в этом случае к координационным, отличающимся меньшей прочностью по сравнению с ковалентными связями. ПВС, обработанный медно-аммиачным раствором, нерастворим как в холодной, так и в горячей воде, но вновь приобретает растворимость после обработки минеральными кислотами или избытком аммиака. Нерастворимые пленки имеют зеленоватый цвет и непрозрачны для ультрафиолетовых лучей.
Подобная обработка с целью придания поливиниловому спирту нерастворимости сопровождается до некоторой степени повышением его хрупкости. Однако устранение хрупкости и повышение гибкости может быть достигнуто добавлением подходящих пластификаторов [15].
6. Криотропное гелеобразование растворов поливинилового спирта.
Известно, что длительное выдерживание концентрированных водных растворов ПВС при комнатных температурах приводит к гелеобразованию.
Если же концентрированные водные растворы ПВС сначала заморозить, а затем после выдерживания в течение некоторого времени оттаять, то вместо прозрачных гидрогелей образуются мутные, упругие, высокоплавкие гетерогенные гели – криогели [16]. Структура и свойства криогелей ПВС (криоПВСГ) зависят от многих факторов, включающих как характеристики самого полимера (концентрация, содержание остаточных О-ацетильных группировок), так и условия низкотемпературного гелеобразования (продолжительность замораживания, скорость замораживания и оттаивания, число циклов перемораживания и др.). Одним из важнейших показателей, определяющих принципиальную возможность формирования криоПВСГ, является содержание в полимере остаточных О-ацетильных группировок [17]. При степени дезацетилирования ниже 90% криоПВСГ не образуется даже при самых благоприятных условиях. Таким образом, сформировать достаточно прочные криогели возможно только на основе концентрированных водных растворов ПВС высокодезацетилированных марок (>97%).
Наиболее существенным фактором, сказывающимся на свойствах криогелей ПВС, является режим размораживания. Было обнаружено [18], что при быстром оттаивании, независимо от условий замораживания исходного раствора и времени экспонирования его при отрицательных температурах, получается не гель, а вязкий и мутный коллоидный раствор. И, наоборот, при медленном размораживании формируются очень упругие криогели.
Медленно оттаявшие образцы более термостабильны и деформируются в меньшей степени.
При рассмотрении структуры ПВС необходимо отметить, что макромолекулы атактических поливиниловых спиртов в водной среде склонны к ассоциации, при этом межмолекулярные водородные связи в основном возникают при участии ОН-групп синдиотактических блоков ПВС, а внутримолекулярные – при участии ОН-групп изотактических фрагментов.
Поэтому криогели на основе ПВС, обогащенного синдиотактическими фрагментами, имеют большую степень кристалличности.
Характерной особенностью полимерного криогеля является его гетерофазная и гетеропористая (очень часто сверхмакропористая или ячеистая) морфология. Порообразователями являются поликристаллы замороженного растворителя. Плавление порогенов после размораживания оставляет в массе криогеля полости, заполняющиеся растаявшим растворителем. Кроме того, в получающемся криогеле макропоры обычно сообщающиеся, поскольку при замерзании каждый кристалл растворителя растет, как правило, от периферии сосуда к центру до соприкосновения с гранью другого кристалла. Криотропное гелеобразование в системах растворитель—полимер—сшивающий агент приводит к получению макропористых криогелей при выдерживании их в замороженном состоянии в течение необходимого времени и с последующим оттаиванием.
КриоПВСГ нашли широкое применение в биотехнологии, медицине, пищевой промышленности и др. Это во многом обусловлено превосходными механическими, диффузионными и теплофизическими свойствами, его не токсичностью и биосовместимостью.
7. Молекулярная структура поливинилового спирта.
Структуру ПВС в основном изучали ренгено- и электронографическими способами. Проведенное Дистлером и Пинскером электронографическое исследование пленок ПВС показало, что на электронограммах в отличие от рентгенонограмм появляются новые рефлексы, которые лежат в направлении параллельном к оси растяжения. По мнению авторов ПВС содержит множество упорядоченных областей различной формы и размеров, внутри которых жесткие участки соседних цепей более или менее правильно взаимоориентированы. Линейные размеры таких упорядоченных областей имеют порядок 10-30 A [19].
В настоящее время нет единого мнения относительно молекулярного периода. Так, Галле и Гофман [20] приводят для молекулярного периода идентичности цифры 2,57 A. По Муни [21], эта величина составляет 2,52 A, из чего вытекает, что углеродная цепь представляет собой плоский зигзаг.
При этом гидроксильные группы находятся по одной стороне цепи, даже, несмотря на то, что в исходном аморфном поливинилацетате эти группы расположены в нерегулярном чередовании справа и слева относительно главной цепи.
Исследование инфракрасных спектров поглощения ПВС Е. Гроссом и Я. Рыскиным [22] при различных температурах осветило вопрос о роли водородной связи. Дифференциальные кривые имеют два максимума: один при ?=3,16 ? и другой при ?=2,79 ?. Первый максимум соответствует колебаниям ОН–групп, «ассоциированных» посредством водородной связи, а второй максимум соответствует колебаниям свободных гидроксильных групп. Таким образом, показано, что в ПВС присутствуют как ассоциированные водородной связью, так и свободные ОН–группы. Причем при комнатной температуре 70% гидроксильных групп находятся в связанном состоянии.
8. Структура и свойства ПВС различной стереорегулярности.
Очевидно, что ПВС, полученный различными методами, различается не только молекулярной массой продукта, но также и его структурой, например, стереорегулярностью полимерных цепей. Чаще встречается атактический ПВС и это напрямую связано с атактической структурой его предтечи поливинилацетата. Атактический ПВС характеризуется достаточно высокой степенью кристалличности (30-40%). При синтезе ПВС из других виниловых эфиров соответствующие образцы показывают большую стереорегулярность. Например, при использовании винилпивалата и винилтрифторацетата, наблюдается слабое увеличение степени синдиотактичности ПВС [23,24], в тоже время, ПВС, полученный из винилбензоата и его производных, имеет повышенное содержание изотактических последовательностей [25].
В синдиотактическом ПВС гидроксильные группы чаще связаны водородными связями, что в свою очередь, приводит к более регулярной упаковке цепей в кристаллитах. В стереорегулярном полимере количество гидроксильных групп, включенных в образование межцепных связей, более значительно по сравнению с теми же группами в атактическом полимере.
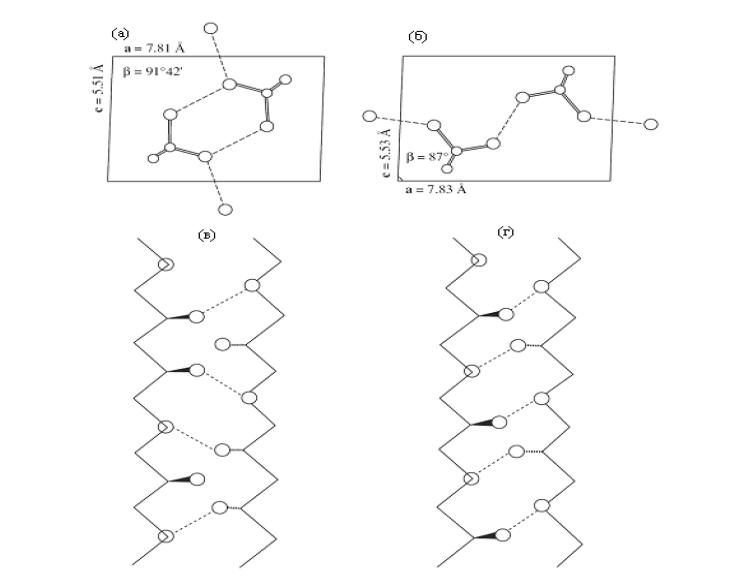
Рис.3. Модели кристаллических решеток Бана (a) и Сакурада (б) в проекции – 010; модель Бана для кристаллической структуры атактического (в) и синдиотактического (г) ПВС (водородные связи показаны пунктирными линиями, гидроксильные группы – пустыми кружочками).
Существуют две альтернативные модели для расчета структуры кристаллической решетки ПВС: модель Бана [26] и модель Сакурада [27, c.60]. Рисунок 3 (а и б) показывает проекции цепей ПВС, полученные для обеих моделей. Как видно, параметры кристаллографической решетки почти одинаковы, однако наблюдается слабое различие ориентации в плоскости транс-зигзаг цепей ПВС относительно кристаллографической оси а и с, что приводит к заметным различиям в направлении водородного связывания.
Согласно модели Сакурада образование водородной связи является двухмерным связыванием в направлении оси ас. Однако, согласно модели Бана цепи связываются в слое bс.
Очевидно, материал с более сильными межмолекулярными цепными взаимодействиями должен характеризоваться не только более высокой температурой плавления, но также улучшенными механическими характеристиками. Температурное поведение ПВС характеризуется термическим расширением в а- и с-направлении. По длине а-оси, коэффициент термического расширения ПВС выше, чем по длине с-оси. Этот результат согласуется с моделью решетки Бана. Как следует из рис. 1.5б, связывание водородными связями существует по длине с-оси, поэтому в этом направлении термическое расширение кристалла является менее очевидным, чем по длине а-оси, где водородная связь не может быть образована.
Таким образом, сравнивание атактический ПВС с ПВС, обладающим повышенным содержанием синдиотактических последовательностей, показывает целый ряд улучшенных свойств: выше точка плавления, выше модуль упругости, выше степень кристалличности и т.д. Более стереорегулярный образец характеризуется более совершенной кристаллической структурой с большими размерами кристаллитов и более плотной упаковкой цепей в кристаллической решетке. Все специфические особенности поведения ПВС с различной стереорегулярной структурой могут быть легко объяснены различной плотностью связывания водородными связями, которая заметно повышается с повышением содержания синдиотактических диад [28].
9. Полиакриламид и его свойства.
Амидная группа обладает значительной полярностью, поэтому амиды хорошо растворимы в воде, а полиакриламид способен сорбировать воду в большом объеме. Амидная группа, содержащая N?H связи, обладает слабокислыми свойствами (Ка составляет около 10-16), т.е. гораздо более кислыми свойствами, чем аммиак (Ка~10-33), что обусловлено высокой степенью стабилизации амидного аниона. Тем не менее, амиды ? это чрезвычайно слабые кислоты, и в практическом плане их следует рассматривать как вещества, лишенные кислых свойств в водном растворе.
Основность амидной группы намного меньше, чем у аминной группы. Так например, основность ацетамина составляет Ка ~10 – 15.
Полиакриламид в водных растворах при комнатной температуре устойчив к гидролизу [29, с. 98], однако при высоких температурах (? 93?С) гидролиз осуществляется с заметной скоростью даже в отсутствие гидролизующих агентов [30].
Реакцию гидролиза ПААм в кислых средах можно упрощенно представить следующей схемой:
В результате щелочного гидролиза ПААм образуются макромолекулы сополимеров акриламида с солями акриловой кислоты. Реакцию щелочного гидролиза полиакриламида можно представить следующей схемой:
В присутствии гидроксида натрия, при 20 ?С можно достигнуть степени гидролиза до 60%.
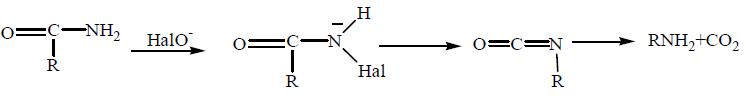
Реакция гипогалоидного расщепления амидов носит название перегруппировки Гофмана и достаточно хорошо изучена на примере низкомолекулярных амидов. Реакцию проводят в присутствии гипогалогенита и щелочи. В качестве гипогалогенита используют гипохлориты и гипобромиты щелочных металлов, причем применение первых более предпочтительно ввиду большей скорости реакции. Схема реакции может быть представлении в следующем виде:
Реакция аминометилирования амидов вторичным амином и формальдегидом носит название реакции Манниха. Ее можно упрощенно представить следующей схемой:
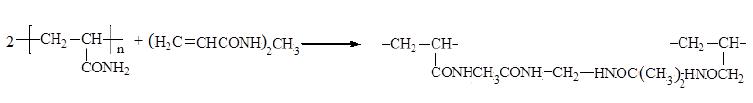
Реакции сшивки ПААм применяют для получения водопоглощающих изделий, пленок, защитных покрытий и капсул для семян, лекарств, удобрений. ПААм можно сшить при взаимодействии с N,N’-метилен-бис- акриламидом
Приведенные данные дают общие представления о химических свойствах полимеров акриламида.
10. Синтез сшитого полиакриламида.
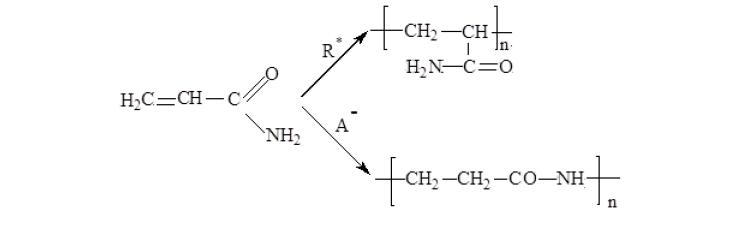
Акриламид легко полимеризуется с образованием линейного высокомолекулярного полимера под действием радикальных и ионных инициаторов, ультрафиолетового и радиационного излучения, ультразвука и электрического тока. Упрощенно радикальная и ионная полимеризация могут быть представлены схемой:
Основным методом синтеза полиакриламида является радикальная полимеризация, которую можно проводить всеми известными способами: в массе кристаллических и расплавленных мономеров, в растворе, эмульсии и суспензии. Каждый из способов имеет свои особенности, обуславливающие свойства полимера.
11. Полиакриламиды и их применение.
Под названием «полиакриламид» обычно объединяют группу полимеров и сополимеров на основе акриламида и его производных.
Полиакриламидные реагенты выпускаются в виде растворов, дисперсий, гранул или порошка с широким диапазоном свойств – в зависимости от назначения могут получаться растворимыми, ограниченно набухающими каучукоподобными гелями и нерастворимыми [31].
Набухший в воде сшитый полиакриламид представляет собой полимерный гель. В состав полиакриламида входит гидрофильная, но не ионогенная амидная группа. Свойства амидной группы имеют важное значение ввиду ее близости к свойствам пептидов и белков – соединений, которые имеют фундаментальное значение для всех известных видов жизни.
Специфические свойства пептидов и белков связаны в первую очередь с их полиамидной структурой. Таким образом, полиакриламид очень близок по природе к белкам, и поэтому не удивительно, что ему уделяется большое внимание исследователями, так как его можно использовать в биологических целях. Необходимо также отметить, что полиакриламид является нетоксичным веществом, поэтому его часто используют в медицине в качестве биоматериалов и лекарственных препаратов.
Полимеры акриламида обладают уникальным комплексом полезных свойств и широко используются в различных областях техники и технологии.
Различные области применения и назначение полимеров показаны в табл. 1.
Таблица 1. Применение полимеров акриламида [32]
| Область применения | Назначение |
| Обработка воды | Флокулянты для очистки природных и промышленных сточных вод, переработки пищевых продуктов. Обезвоживающие агенты для осадков |
| Обработка бумаги | Регуляторы прочности бумаги в сухом и влажном состоянии, добавки для улучшения качества и печатных свойств бумаги |
| Добыча и обработка полезных ископаемых | Флокулянты хвостов флотации руд, при обогащении и регенерации полезных ископаемых. Уменьшение запыленности в угольных шахтах, при бурении, на асбестовых заводах |
| Добыча нефти | Стабилизаторы, регуляторы фильтруемости и реологических свойств буровых растворов |
| Сельское хозяйство | Структурообразователи почв для укрепления стенок скважин при вторичной добыче нефти Структурообразователи почв Пленкообразователи для семян, удобрений, инсектицидов, гербицидов и фунгицидов |
| Медицина | Суперабсорбенты для средств гигиены Пленкообразователи для фармацевтических препаратов пролонгированного действия Гидрогели для контактных офтальмологических линз, пластической хирургии |
В группу «полиакриламидов» входят полиакриламид – неионогенный полимер: , 
его анионные производные, например, частично гидролизованный полиакриламид
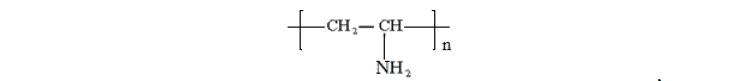
, и катионные производные, например, поливиниламин
Эффективность применения полимеров акриламида определяется их характеристиками. Основное применение неионогенных полимеров – очистка природных и сточных вод и обезвоживание осадков в целлюлозно- бумажной промышленности, анионных полимеров – водообработка, флокуляция хвостов флотации руд, обогащение и регенерация полезных ископаемых и нефти, обработка бумаги и шлихтование текстильных материалов. Катионных полимеров – обработка бумаги и флокуляция биологических клеток. В зависимости от методики синтеза можно варьировать наличие определенных групп и, соответственно, свойства получаемого полимера.
ЛИТЕРАТУРА
1. Папков С.П., Диброва А.К. К проблеме самопроизвольного застудневания растворов полимеров.// Высокомол. соед. 1983. Т. 25 А. С. 630-635.
2. Ушаков С.Н. Поливиниловый спирт и его производные. М.-Л.: Акад. Наук СССР. 1960. Т. 1. 552 с.
3. Энциклопедия полимеров. М.: Советская энциклопедия. 1974. Т.
4. Ямсков И.А., Буданов М.В., Даванков В.А. Гидрофильные носители на основе поливинилового спирта для иммобилизации ферментов.// Биоорганическая химия. 1979. Т. 5. № 11. С. 1728-1734.
5. Ямсков И.А., Буданов М.В., Даванков В.А. Координационно-ионная иммобилизация ферментов. Связывание пенициллинаминогидролазы через комплексы меди.// Биоорганическая химия. 1979. Т. 5. № 5. С. 757-767.
6. Bo, Jiang. Study of pole (vinil alcohol) hydrogel crosslinked by epichlorhydrin.// Chem. Abs. 1993. V. 118. № 5. P. 33. (23107j).
7. Nagy N., Horkay F. A simple and accurate method for the determination of solvent activity in swollen gels.// Acta Chim. Acad. Sci.Hung. 1980. V. 104. №1. P. 49-61.
8. Зубов П.И., Осипов Е.А., Сухарев Л.А. Исследование структурообразования в растворах поливинилового спирта.// Высокомол. соед. 1964. T. 6. № 5. C. 811- 817.
9. Jackson J.F., Gills J. Stain birefringence of poly (vinil alcohol) gels.// J. Polym. Sci. 1967. A-2. V. 5. № 4. P. 795-798.
10. Bashaw J., Smith K.J. Thermoelastic properties of networks in swelling equilibrium: poly (vinil alcohol).// J. Polym. Sci. 1968. A-2. V. 6. № 6. P.1051-1063.
11. Donersloot M.C.A., Gouda J.H., Aarsen J.J. Prina W. Polymer gel strycture elucidation by means of light scattering and photo-elasticity.// Recuel Trav. Chim. 1967. V. 86. № 4. P. 321-340.
12. Abe H., Prins W. Elasticity of poly (vinil alcohol) filaments in swelling equilibrium with water.// J. Polym. Sci. 1963. V. 6. № 6. P. 527-546.
13. Horkay F., Nagy N. Mechanical-reological studies of polymer networks. I. Effect of conditions of cross-linking on the mechanical properties.// Acta Chim. Acad. Hung. 1981. V. 107. № 4. P. 321-334.
14. Rhim, Ji Won, Sohn, Min Joung, Joo, Hyeok Jong, Lee, Kew Ho. Pervaporation separation of binary organic-aqueous liquid mixtures using crosslinked PVA membranes. I. Characterization of the reaction between PVA and poly (acrylic acid).// Chem. Abs. 1993. V. 119. № 20. P. 77. (20489h).
15. Cheng A.T.J., Rodrignes F. Mechanical properties of borate crosslinked poly (vinil alcohol) gels.// J. Appl. Polym. Sci. 1981. V. 26. № 11. P. 3895-3908.32. Saito Okayama. Die Adsorption von Kupfer auf Polyvinylalkohol.// Kolloid. Z. 1954. Bd.
139. H. 3. S. 150-155.
16. Лозинский В.И. Криотропное гелеобразование растворов поливинилового спирта.// Успехи химии. 1998. T. 67. №7. С. 641-655.
17. Лозинский В.И. Криогели на основе природных и синтетических полимеров: получение, свойства и области применения.// Успехи химии. 2002. T. 71. №6. С. 559-584.
18. Домотенко Л.В. Криогели поливинилового спирта: получение и свойства. Дисс… канд. хим. наук. Москва. ИНЭОС АН СССР. 1986. 173 с.
19. Журков С., Левин Б. ДАН СССР. 1950. V. 77. C. 269-270.
20. Halle F. Rontgenoskopie organischer Gele.// Kolloid Z. 1934. Bd. 69. H. 3. P. 324- 337.
21. Mooney R.C.L. An X-Ray Study of the Structure of Polyvinyl Alcohol.// J. Am. Chem. Soc. 1941. V. 63. № 10. P. 2828-2832.
22. Гросс. Е., Рыскин Я. Сборник, посвященный 70-летию акад. А.Ф. Иоффе. Изд. АН СССР, 1950. с. 249.
23. Lyoo W.S., Ha W.S. Preparation of Syndiotacticity-Rich High Molecular Weight Polyvinyl Alcohol Microfibrillar Fiber by Photoinitiated Bulk Polymerization and Saponification.// J. Polym. Sci., Polym. Chem. Ed. 1997. V. A35. №1. P.55-67.
24. Yamaura K., Mizutani K., Monma N., Tanigami N. and Matsuzava S., J. Appl. Polym. Sci. 1986. V. 31. № 2. Р. 521.
25. Imai K., Shiomi T., Tezuka Y., Kawanishi T., Jin T. Polyvinyl Alcohol Obtained throught Polymerization of Some Vinyl Esters.// J.Polym. Sci., Polym. Chem. Ed., 1988. V. 26. №.7. P. 1961-1968.
26. Bunn C.W. Nature. 1948. V. 161. №4102. p. 929 цит. по Yurovskikh S.V., Chvalun S.N., Lyoo W.S. Structure and Properties of Poly (vinyl alcohol) of Different Stereoregularity. Polymer Sience. 2001. V.43. №3. P.278-284.
27. Sakurada I. Polyvinyl Alcohol Fibers. New York: Wiley. 1991. 312p.
28. Билобров В.М. Водородная связь. Внутримолекулярные взаимодействия. Киев: Наук. думка. 1991. 320с.
29. ВейцерЮ.И., Минц Д.М. Высокомолекулярные флокулянты в процессах очистки сточных вод. М.: Стройиздат, 1984. 201 с.
30. Зильберман Е.Н., Старков А.А., Еремеев Н.В., Траченко В.И., Колесников В.А. Высокотемпературный гидролиз полиакриламида.//Высокомолек. cоед. Серия Б.
1979. T. 21. № 1. C. 30-33.
31. Куренков В.Ф. Водорастворимые полимеры акриламида.//Соросовский образовательный журнал. 1997. № 5. C. 48-53 32. Полиакриламид. (Под ред. В.Ф.Куренкова). М.: Химия. 1992. 192 с.