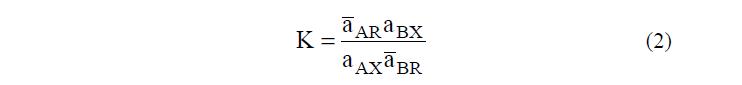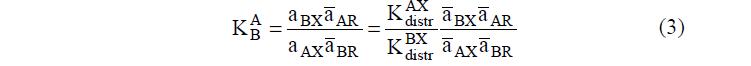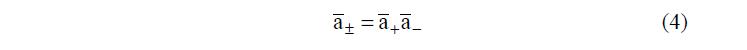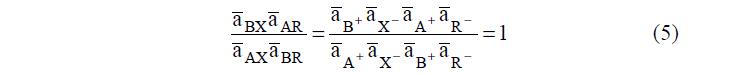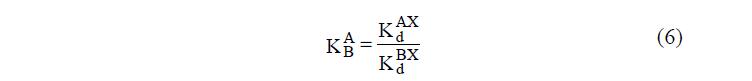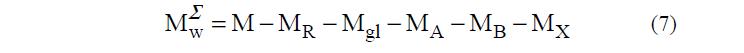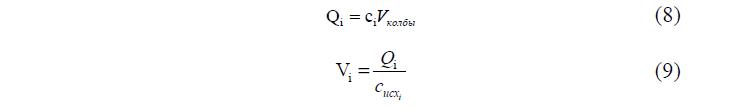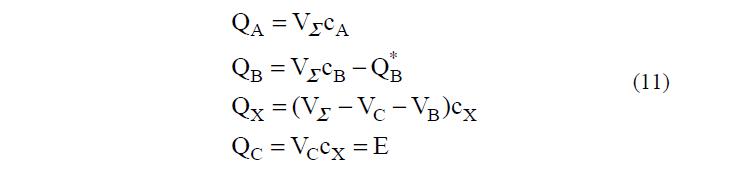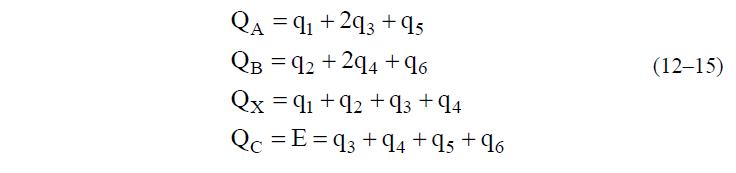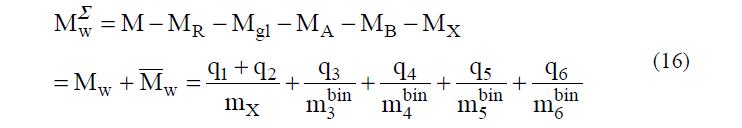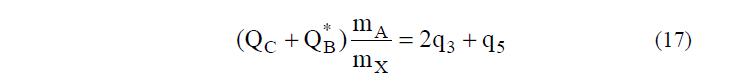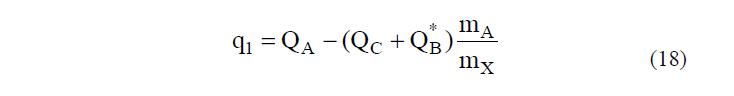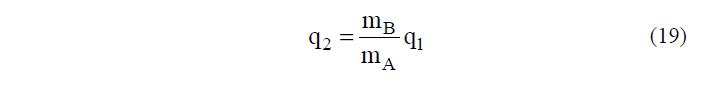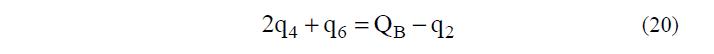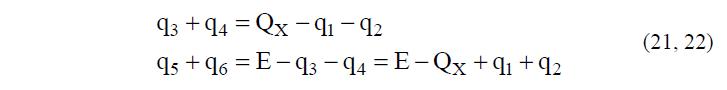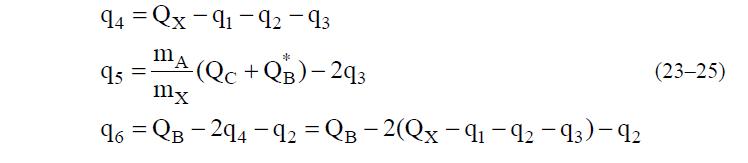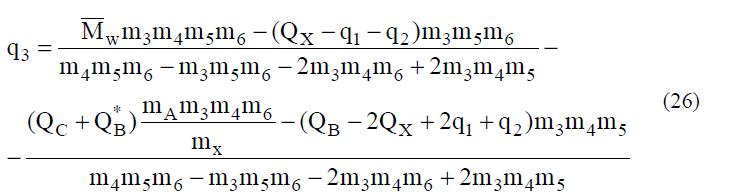Физическая химия полимерных гелей Лекция 16 ОПИСАНИЕ МЕЖФАЗОВОГО РАВНОВЕСИЯ В СИСТЕМЕ ИОНИТ – РАСТВОР. КОНСТАНТА ИОНООБМЕННОГО РАВНОВЕСИЯ.

Физическая химия полимерных гелей Лекция 15 ВЗАИМОДЕЙСТВИЕ РАСТВОРЕННЫХ ВЕЩЕСТВ С ПОЛЯРНЫМИ ГРУППАМИ. КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ РАСТВОРЕННЫХ ВЕЩЕСТВ В ПОЛИМЕРНЫХ ГЕЛЯХ.
19.12.2015
Физическая химия полимерных гелей Лекция 17 ВЛИЯНИЕ СВОЙСТВ КОНТАКТИРУЮЩИХ ФАЗ НА ОБЪЕМ ФАЗЫ ВР В ПГ. ЧАСТЬ 1.
19.12.2015Физическая химия полимерных гелей Лекция 16 ОПИСАНИЕ МЕЖФАЗОВОГО РАВНОВЕСИЯ В СИСТЕМЕ ИОНИТ – РАСТВОР. КОНСТАНТА ИОНООБМЕННОГО РАВНОВЕСИЯ.
Физическая химия полимерных гелей
Ферапонтов Н. Б., Гагарин А. Н., Струсовская Н. Л., Токмачёв М. Г., Тробов Х.Т., Рубин Ф.Ф.
Москва, МГУ имени М. В. Ломоносова 2015 г.
В этой лекции речь пойдет о том, как определить константу ионообменного равновесия в системах, где есть ионный обмен и НМЭ проникают в фазу ПР. Пусть в исследуемой системе проходит реакция:
В этом случае выражение для константы равновесия будет иметь вид:
Если при равновесии со смешанными растворами НМЭ ионит находится в смешанной ионной форме и фаза ПР содержит два НМЭ, распределение воды и электролитов между фазами также описывается с помощью констант распределения. Сорбция электролитов ионитом, очевидно, оказывает влияние на равновесие ионного обмена. Соответственно, между константой равновесия ионного обмена и константами распределения необменно сорбированных электролитов должна существовать связь. Снова запишем константу равновесия. Получим:
Записав активности в виде ионных произведений
и подставив их в правую часть уравнения (3), получим, что произведение активностей реагирующих веществ строго равно единице:
Отсюда следует, что константа ионообменного равновесия для таких систем есть ни что иное, как отношение констант распределения электролитов:
Как видно, в выражение для константы равновесия ионного обмена не входят величины, явно связанные со свойствами ионообменных групп. Из этого можно сделать вывод, что константы распределения (являющиеся, как и все константы, мерой нашего незнания свойств системы) учитывают свойства полярных групп в ионите.
В рамках модели имеется возможность экспериментального определения активности компонентов в фазе ПР и, следовательно, константы ионообменного равновесия. Результаты такого экспериментального исследования представлены в работе [1]. Они показали удовлетворительное согласие расчета и эксперимента.
1. Экспериментальное определение количеств и свойств компонентов в фазах.
Для того чтобы получить информацию о равновесном распределении компонентов между фазами удобнее всего воспользоваться колоночным методом изучения ионообменных систем. С помощью методики, описанной в лекции 12 и гетерофазной модели (лекция 7), попробуем определить распределение компонентов в системах, в которых имеют место как сорбция НМЭ, так и ионный обмен.
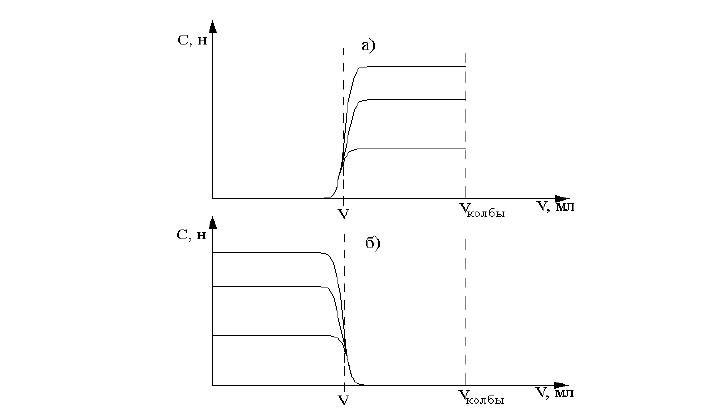
В простейшем случае, когда колонка (см. лекцию12) заполнена инертной к раствору фазой (например, стеклянными шариками) и водой, пропускание через нее раствора любого вещества и состава приведет к одному и тому же результату: будут получены «выходные кривые» (рис. 1), с помощью которых можно определить объем V, занимаемый водой в исследуемой системе. Точно такой же результат будет получен и в «обратном опыте», когда раствор из колонки будет вытеснен водой (рис. 1б).
Рис. 1. Выходные кривые: а) – прямой опыт; б) –обратный опыт.
Рис. 2. Влияние концентрации раствора на занимаемый им объем.
Если в колонку загрузить ионит AR, который препятствует проникновению НМЭ в фазу ПР, то, пропуская через колонку растворы электролита AX разных концентраций, увидим, что величина V? увеличи- вается с ростом концентрации пропускаемого раствора (рис. 2). Это происходит потому, что с увеличением концентрации AX уменьшается активность воды в этом растворе, что приводит к уменьшению количества воды в фазе ПР. То есть увеличение объема раствора AX происходит в результате уменьшения объема ПР. Влияние активности воды во внешнем растворе на количество воды в фазе ПР описывается с помощью константы распределения воды Kw d , что хорошо подтверждается данным экспериментом.
Если НМЭ проникает в фазу ПР, то, как показано в лекции 15, это происходит в результате взаимодействия молекулы НМЭ с ионообменной группой. Количество воды, окружающей образованный ассоциат, соответствует концентрации раствора данного НМЭ при активности воды, равной активности воды в ПР. Следовательно, в результате такого проникновения вода, которая находилась около ионообменной группы, переходит во внешний раствор. Кроме того, в результате перехода НМЭ в фазу ПР, также выделяется дополнительное количество воды. В колоночном эксперименте эти два процесса приводят к заметному увеличению величины V. С помощью методик, описанных в работе [2], этим методом изучали сорбцию НМЭ сшитыми полиэлектролитами.
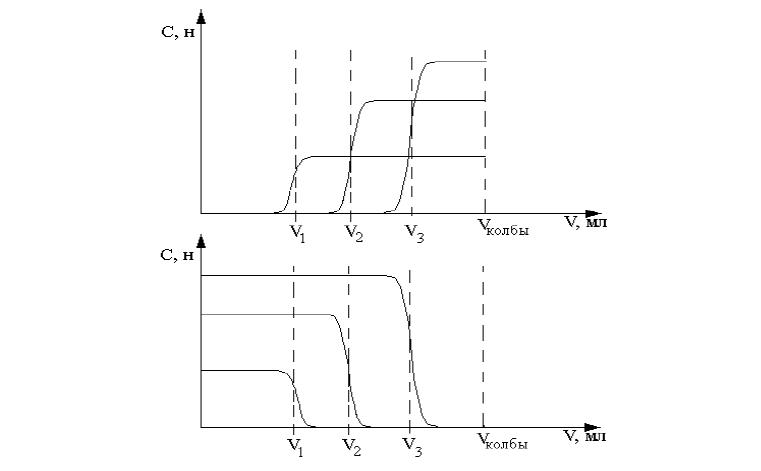
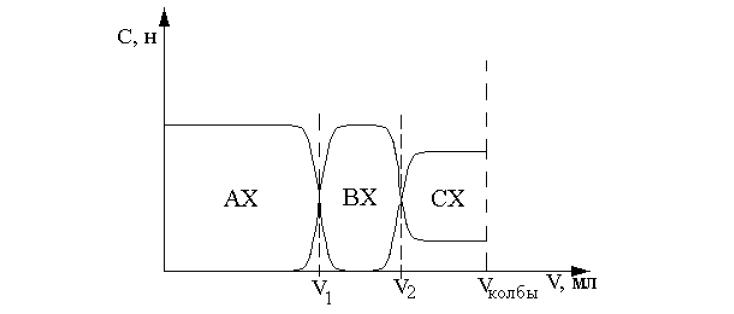
Если через колонку с ионитом, находящимся в RA-форме пропустить раствор электролита BX, то, собирая и анализируя фильтрат, получим зависимость состава и концентрации фильтрата от объема пропущенного раствора (рис. 4). Этих данных достаточно, чтобы определить обменную емкость ионита и занимаемый им объем. В более сложном случае, когда через колонку пропускают раствор, содержащий два электролита BX, CX анализ фильтрата (рис. 5) позволяет не только определить обменную емкость, но и соотношение ионных форм при равновесии с данным раствором.
Рис. 4. Ионообменное вытеснение иона А ионом В.
Рис. 5. Фронтальное ионообменное вытеснение иона А смесью ВХ+СХ.
Таким образом, обрабатывая экспериментальные результаты, полученные колоночным методом, можно получить довольно полную информацию о количестве и составе фазы ПР.
2. Определение состава фазы полимерного раствора.
Для проведения экспериментов, где присутствует ионный обмен, и разделяемые электролиты проникают в фазу ПР, удобно использовать колонку, объемом около 200 мл. Перед проведением эксперимента ионит переводят в CR-форму, то есть в форму иона С, и отмывают от электролита водой. Затем через отмытую колонку пропускают исследуемый раствор, содержащий два электролита AX BX. Концентрации и активности компонентов этого раствора должны быть известны. Фильтрат собирают в мерную колбу. Ее объем должен быть достаточен для того, чтобы привести ионит в равновесие с исследуемым раствором. Равновесие наступает после того как в фильтрате концентрации ионов А и В становятся равными исходной концентрации.
Для того чтобы определить массу воды в колонке, ее взвешивают.
Затем в колбе определяют концентрации ионов А, В и С и с помощью уравнений 8 и 9 вычисляют количества этих ионов QА, * QB и QС и объемы растворов VС и VВ, в которых эти ионы вышли из колонки колбы
По результатам расчетов строят график (рис. 6) Надо отметить, что величина QС численно равна обменной емкости ионита в колонке Е. Кроме того, объем VB, содержащий менее селективный к иониту ион В, вместе с объемом раствора VС, содержащим ион С, показывают какое количество исходного раствора необходимо для того, чтобы ионит пришел в равновесие с исследуемым раствором.
Рис. 6. Объемы и составы фильтрата, полученные в результате эксперимента.
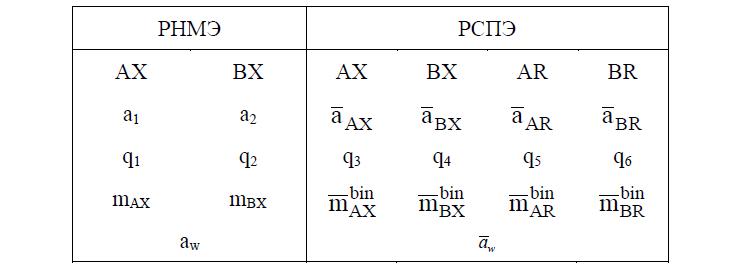
Чтобы определить количества компонентов (ионов) в колонке, находящейся в равновесии с исходным раствором: QA, QB и QX запишем следующие выражения:
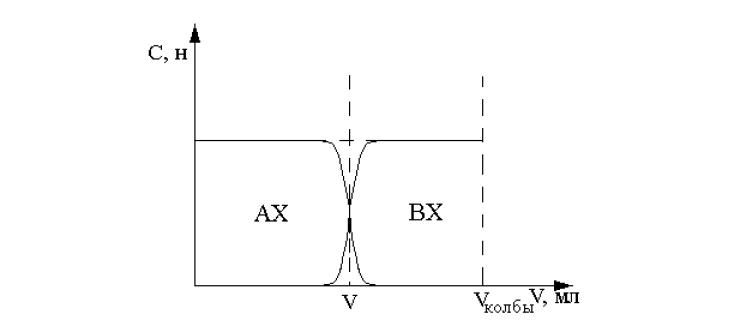
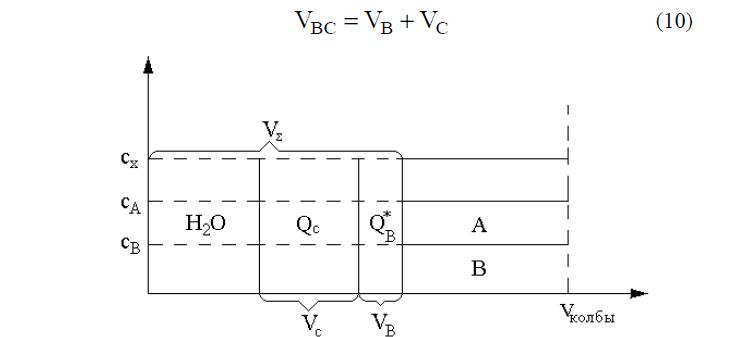
Эти величины также как и масса воды Mw потребуются для определения составов фаз. На рис. 7 показано, как в этом случае распределены компоненты между фазами.
Рис.7. Схема строения системы ионит-раствор.
Чтобы определить константу ионообменного равновесия необходимо знать активности соединений, принимающих участие в реакции обмена: ХА, ХВ, RA и RB. Для этого надо найти количество каждого из этих веществ в фазе ПР. Ниже представлен алгоритм такого расчета. Вначале запишем уравнения, связывающие определенные из эксперимента величины с параметрами модели.
Как уже говорилось выше, количество иона А, находящееся в фазе ПР при равновесии с исследуемым раствором, можно рассчитать исходя из объема раствора VВ+VС, который вышел из колонки до появления в фильтрате иона А:
Сравнивая это выражение с (12) находим q1:
Количество иона В, находящегося в колонке в фазе ПР, вычисляют, принимая во внимание исходную концентрацию раствора
а количество В в фазе ПР с учетом (13) будет
Преобразуя (14) и (15) запишем:
Воспользовавшись уравнением (21) выразим q4, величину q5 определим из (17), а q6 найдем из (20).
Все это подставим в (16) и получим уравнение с одним неизвестным q3
Несмотря на большое количество величин в этом уравнении, все они известны, поэтому определение величины q3 и всех остальных не вызывает проблем. После того как количества компонентов в фазе ПР определены, нет препятствий для нахождения их активностей. Таким образом, на основании экспериментальных результатов можно вычислить константу равновесия в исследуемой системе.