Физическая химия полимерных гелей Лекция 6 ТЕОРИИ И МОДЕЛИ, ОПИСЫВАЮЩИЕ СВОЙСТВА ПОЛИМЕРНЫХ РАСВОРОВ И ГЕЛЕЙ

Физическая химия полимерных гелей Лекция 5 МЕТОДЫ ИССЛЕДОВАНИЯ КОЛИЧЕСТВ И СВОЙСТВ ВОДЫ В ПОЛИМЕРНЫХ ГЕЛЯХ
29.11.2015Физическая химия полимерных гелей Лекция 7 ГЕТЕРОФАЗНАЯ МОДЕЛЬ СТРОЕНИЯ ПОЛИМЕРНОГО ГЕЛЯ
08.12.2015Физическая химия полимерных гелей Лекция 6 ТЕОРИИ И МОДЕЛИ, ОПИСЫВАЮЩИЕ СВОЙСТВА ПОЛИМЕРНЫХ РАСВОРОВ И ГЕЛЕЙ
Физическая химия полимерных гелей
Ферапонтов Н. Б., Гагарин А. Н., Струсовская Н. Л., Токмачёв М. Г., Тробов Х.Т., Рубин Ф.Ф.
Москва, МГУ имени М. В. Ломоносова 2015 г.
В 1941-1953 гг. вышли в свет работы П. Флори [1 – 10], в которых были математически описаны условия, приводящие к образованию трехмерной молекулярной сетки, образующейся в результате реакции поликонденсации, а также изложена теория растворов полимеров. Независимо от него к аналогичным выводам пришел М. Хаггинс [11].
Теория растворов полимеров Флори – Хаггинса основана на предполо- жении о том, что сегмент макромолекулы в растворе низкомолекулярного соединения (НМС) ведет себя подобно последнему, если они близки по химической природе. То есть энергия взаимодействия между сегментом макромолекулы и молекулой НМС близка к энергии взаимодействия между молекулами этого НМС в растворе. Тогда теплота смешения будет близка к нулю и, таким образом, термодинамические свойства раствора будут определяться изменением энтропии смешения.
Для описания растворов полимеров обоими авторами была использована решеточная модель, в которой принимается, что макромолекула занимает некоторое количество ячеек в решетке, а молекула растворителя – одну. Причем длина сегмента макромолекулы, занимающая одну ячейку, равна длине молекулы НМС. Исходя из этих положений, можно рассчитать число конформаций, доступных каждой цепи, и термодинамическую вероятность состояния раствора, выражаемую произведением числа способов размещения всех цепей и всех молекул растворителя. После ряда преобразований было получено уравнение для расчета энтропии смешения: 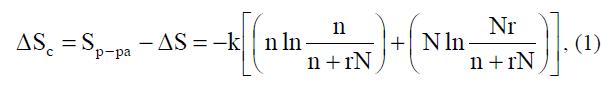 где N – число цепей полимера, n – число молекул растворителя, k – постоянная Больцмана, ΔS – энтропия разориентации гипотетического «упорядоченного» полимера, энтропия которого принимается равной нулю.
где N – число цепей полимера, n – число молекул растворителя, k – постоянная Больцмана, ΔS – энтропия разориентации гипотетического «упорядоченного» полимера, энтропия которого принимается равной нулю.
Считая, что n rN 1 n = φ + и 2 n Nr Nr = φ + – объемные доли растворителя и полимера, 2 1 V V r = – отношение молярных объемов полимера и растворителя, для 1 моля мест в решетке получим: 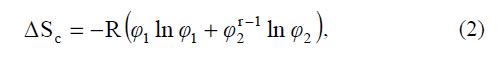 где R – универсальная газовая постоянная.
где R – универсальная газовая постоянная.
Вместе с тем наличие тепловых эффектов при набухании указывало на более сильные взаимодействия, чем простое раздвижение цепей и изменение конформационного набора. Поэтому для расчета теплоты смешения были учтены парные взаимодействия в чистых растворителе и полимере (w11, w22), которые отличаются от энергии взаимодействия полимер – растворитель (w12) на величину ( ) 12 11 22 12 w w w 2 1 Δw = + — : 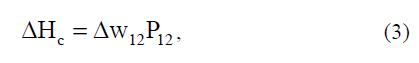 где Р12 – среднее число контактов растворитель – полимер, которое не может быть определено в рамках теории. Поэтому Флори ввел безразмерный параметр (c), характеризующий избыточную свободную энергию взаимодействия, приходящуюся на 1 молекулу растворителя в растворе.
где Р12 – среднее число контактов растворитель – полимер, которое не может быть определено в рамках теории. Поэтому Флори ввел безразмерный параметр (c), характеризующий избыточную свободную энергию взаимодействия, приходящуюся на 1 молекулу растворителя в растворе.
Каждая молекула растворителя имеет zj2 соседних молекул полимера, тогда теплота смешения n1 молекул растворителя c Nr сегментами полимера будет записана следующим образом: ![]() Рассчитав свободную энергию смешения, можно вычислить изменение химического потенциала растворителя (m1) в растворе по сравнению с его значением в чистом растворителе ( о μ1 ), которое связано с экспериментально определяемыми характеристиками раствора – осмотическим давлением (p) и давлением паров растворителя над раствором (или гелем):
Рассчитав свободную энергию смешения, можно вычислить изменение химического потенциала растворителя (m1) в растворе по сравнению с его значением в чистом растворителе ( о μ1 ), которое связано с экспериментально определяемыми характеристиками раствора – осмотическим давлением (p) и давлением паров растворителя над раствором (или гелем): 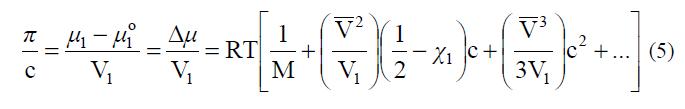 где: V – удельный парциальный объем полимера, М – его молекулярная масса, V c φ2 = – концентрация полимера в растворе. Это уравнение написано для малых концентраций раствора, когда ln(1–j2) можно разложить в ряд по степенямj2. Или:
где: V – удельный парциальный объем полимера, М – его молекулярная масса, V c φ2 = – концентрация полимера в растворе. Это уравнение написано для малых концентраций раствора, когда ln(1–j2) можно разложить в ряд по степенямj2. Или: 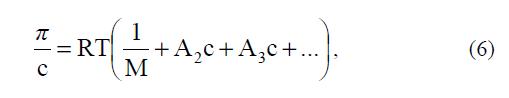 где: А2, А3 и т.д. – так называемые вириальные коэффициенты, характеризую- щие отклонение полимерных растворов от идеальности. Второй вириальный коэффициент можно определить экспериментально по зависимости p от с, а также методами светорассеяния, седиментации и др.
где: А2, А3 и т.д. – так называемые вириальные коэффициенты, характеризую- щие отклонение полимерных растворов от идеальности. Второй вириальный коэффициент можно определить экспериментально по зависимости p от с, а также методами светорассеяния, седиментации и др.
Для очень разбавленных растворов полимеров эта теория неприменима, так как в таких растворах существуют области, резко различающиеся по концентрации полимерных сегментов: одни содержат чистый растворитель, а другие – набухшие в растворителе полимерные клубки. Нужно было учитывать неоднородную структуру раствора. Это привело к появлению понятий q – температуры и исключенного объема (u) – объема, из которого данная макромолекула вытесняет все остальные. Чем сильнее «набухает» макромолекула, то есть чем больше 2 A 2 2M N u A = , тем больше исключенный объем. Эти характеристики раствора можно учесть, если рассматривать параметр взаимодействия Флори – Хаггинса состоящим из двух частей: энтропийной и энергетической. q – температура, при которой эти два фактора уравновешивают друг друга, и клубок принимает невозмущенные размеры, то есть коэффициент набухания макромолекулы 1 R R 2 o 2 α = = , где 2 o R – радиус инерции макромолекулы, а R2 – радиус инерции макромолекулы в набухшем состоянии. Коэффициент набухания связан со вторым вириальным коэффициентом следующим соотношением: 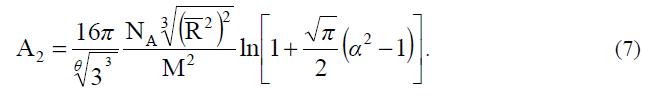 В х о р о ш е м растворителе А2 всегда больше 1 и a>1, то есть силы отталкивания преобладают над силами притяжения. Макромолекула полимера как бы растягивается, принимая в себя растворитель. У х у д ш а я качество растворителя, можно получить Т=q и А2=0, тогда a=1, и даже Т<q, А2 Теория Флори – Хаггинса позволила описать термодинамические свойства растворов полимеров, но из нее следовало, что гибкость цепи не зависит от природы растворителя, хотя это утверждение неверно. Кроме того, эксперимент показывает иную, чем по теории, зависимость А2 от a.
В х о р о ш е м растворителе А2 всегда больше 1 и a>1, то есть силы отталкивания преобладают над силами притяжения. Макромолекула полимера как бы растягивается, принимая в себя растворитель. У х у д ш а я качество растворителя, можно получить Т=q и А2=0, тогда a=1, и даже Т<q, А2 Теория Флори – Хаггинса позволила описать термодинамические свойства растворов полимеров, но из нее следовало, что гибкость цепи не зависит от природы растворителя, хотя это утверждение неверно. Кроме того, эксперимент показывает иную, чем по теории, зависимость А2 от a.
Дальнейшее развитие теории растворов полимеров шло по пути учета изменения объемов при смешении полимера и растворителя.
Взаимодействие полиэлектролитов с растворами низкомолекулярных электролитов.
Традиционный термодинамический подход к описанию распределения ионов между СПЭ и равновесным раствором электролита основан на соотношении Доннана [12, с.129-137]. Большинство последующих теорий [13- 20] набухания полиэлектролитов в растворах электролитов было построено именно на нем, причем СПЭ рассматривался как гомогенная система, состоящая из двух компонентов: собственно СПЭ и содержащейся в нем воды.
Суть теории Доннана [21,22] заключается в том, что ионы, не способные проходить через полупроницаемую мембрану, тем не менее, влияют на распределение ионов, проникающих через нее. Причем причины, препятствующие перемещению ионов через границу, несущественны.
Равновесие, устанавливающееся в такой системе, называется мембранным.
Оно характеризуется не только разностью осмотических давлений, но и разностью электрических потенциалов по обе стороны мембраны, а также разными концентрациями электролитов.
Выражение для электрохимических потенциалов иона в фазах раствора ( μi ) и СПЭ ( μi ) представлено уравнениями: 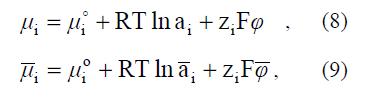 где o μi – стандартное значение химического потенциала в растворе; j и j – электрические потенциалы в растворе и в фазе СПЭ; i a и i a – активности ионов i в растворе и в фазе СПЭ; zi – число зарядов компонента i, F – число Фарадея, R – газовая постоянная, T – температура. Стандартное значение химического потенциала ионов в СПЭ такое же, как и в растворе. Приравнивая затем значения mi и μi отдельно для катионов (+) и анионов (–) и исключая разность электрических потенциалов (φ–j), получают соотношение Доннана:
где o μi – стандартное значение химического потенциала в растворе; j и j – электрические потенциалы в растворе и в фазе СПЭ; i a и i a – активности ионов i в растворе и в фазе СПЭ; zi – число зарядов компонента i, F – число Фарадея, R – газовая постоянная, T – температура. Стандартное значение химического потенциала ионов в СПЭ такое же, как и в растворе. Приравнивая затем значения mi и μi отдельно для катионов (+) и анионов (–) и исключая разность электрических потенциалов (φ–j), получают соотношение Доннана: 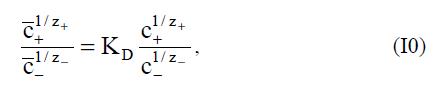 где с+ и c– – концентрации ионов во внешнем равновесном растворе, z+c+ = -z-c- = с – концентрация электролита в растворе (г-экв/л); c+ и c- – концентрации ионов в СПЭ, связанные условием электронейтральности:
где с+ и c– – концентрации ионов во внешнем равновесном растворе, z+c+ = -z-c- = с – концентрация электролита в растворе (г-экв/л); c+ и c- – концентрации ионов в СПЭ, связанные условием электронейтральности:  где Е – обменная емкость СПЭ, KD – “константа” Доннана, которую выражают через коэффициенты активности ионов в растворе (γi ) и в полиэлектролите (γi ) следующим образом:
где Е – обменная емкость СПЭ, KD – “константа” Доннана, которую выражают через коэффициенты активности ионов в растворе (γi ) и в полиэлектролите (γi ) следующим образом: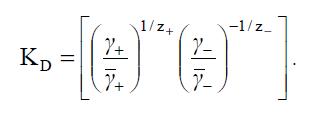
Или:  где ( ) ν ν ν γ γ γ 1/ + — ± = + — и ( ) ν ν ν γ γ γ 1/ + — ± = + — – средние моляльные коэффициенты активности электролита в растворе и в СПЭ; ν = ν+ + ν- – число ионов.
где ( ) ν ν ν γ γ γ 1/ + — ± = + — и ( ) ν ν ν γ γ γ 1/ + — ± = + — – средние моляльные коэффициенты активности электролита в растворе и в СПЭ; ν = ν+ + ν- – число ионов.
Между фазами раствора и полиэлектролита устанавливается разность потенциалов, называемая мембранным потенциалом: 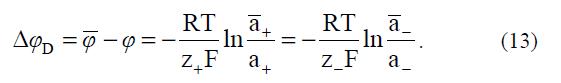 Из теории Доннана следует три основных вывода о состоянии равновесия в системе: · обычно фаза СПЭ обеднена поглощенным электролитом по сравнению с раствором (отрицательная сорбция). Положительная сорбция возможна только в случае большего сродства СПЭ к электролиту, чем у раствора; · концентрация поглощенного электролита в СПЭ меньше у СПЭ с большей емкостью, большей степенью сшивки и с меньшей степенью набухания; · соотношение концентраций поглощенного и оставшегося в растворе электролита существенно зависит от валентного типа электролита. При малых концентрациях равновесного раствора электролит, имеющий большее отношение X A z z , присутствует в СПЭ в значительно меньших количествах.
Из теории Доннана следует три основных вывода о состоянии равновесия в системе: · обычно фаза СПЭ обеднена поглощенным электролитом по сравнению с раствором (отрицательная сорбция). Положительная сорбция возможна только в случае большего сродства СПЭ к электролиту, чем у раствора; · концентрация поглощенного электролита в СПЭ меньше у СПЭ с большей емкостью, большей степенью сшивки и с меньшей степенью набухания; · соотношение концентраций поглощенного и оставшегося в растворе электролита существенно зависит от валентного типа электролита. При малых концентрациях равновесного раствора электролит, имеющий большее отношение X A z z , присутствует в СПЭ в значительно меньших количествах.
Преимущества теории Доннана, примененной к описанию систем СПЭ – НМЭ состоят во внешней простоте и наглядности исходных предпосылок, отсутствии в них спорных эмпирических допущений, строгости термодинамического вывода ее следствий. Она правильно в целом представляет картину в системе СПЭ – раствор на качественном уровне, но неудовлетворительно описывает распределение электролита между фазами количественно. Развитый на ее основе метод расчета существенно занижает количество сорбированного электролита по сравнениюс экспериментальными данными. Эти расхождения наиболее заметны в области растворов с высокими концентрациями, где поправки на необменную сорбцию более всего сказываются на практике [23, с.23 – 32.]. Исходя из полученных эксперимен- тальных результатов, Е. Глюкауф [24] сделал вывод о том, что органические СПЭ не могут считаться гомогенными.
Представления Доннана были положены в основу модели В. Баумана и Дж. Эйхгорна [25], в которой на примере сульфокатионита Дауэкс-50 и HCl показано, что роль каркаса сводится к ограничению подвижности фиксированных ионов, а давление набухания никак не учитывается. Ценность этой модели состоит в том, что она проводит аналогию между фазой СПЭ и водными растворами электролитов.
В работах Г. Грегора [26, 27] утверждалось, что решающее влияние на набухание СПЭ оказывает способность ионов к сольватации, поэтому в модели автор рассматривал не просто ионы, а сольватированные подвижные ионы и «свободный» растворитель. Цепи полимера были представлены упругими пружинами. Из-за разности осмотических давлений во внешнем растворе и в полиэлектролите при их контакте в поры полиэлектролита перемещаются ионы, увеличивая при этом размер пор и растягивая пружины.
Равновесие наступит при равенстве этих сил. Ни энергия взаимодействия соседних участков цепи, как у С. М. Липатова и С. И. Меерсон, ни энропийный фактор (П. Флори) не учитывались. Однако модель не объясняла избирательной сорбции, а также аномалий, вызванных образованием химических связей или ионных пар.
В более поздней модели Лазара – Грегора [цит. по 3, с.110] уже рассматривались силы электростатического отталкивания ионов в самом СПЭ.
Введя ряд допущений, авторы получили сложные уравнения, имеющие только численные решения, которые, тем не менее, удовлетворительно объяснили экспериментально наблюдаемые изменения в степенях набухания полиэле- ктролитов в зависимости от концентрации раствора и природы противоионов, а также уменьшение коэффициента активности с разбавлением раствора.
В 1956 г. вышла работа С. Райса и Ф. Гарриса [28], в которой авторы рассматривали СПЭ как гели полиэлектролитов, образованные цепями из гибко соединенных жестких заряженных сегментов. При таком подходе не учитывались ни механическая упругость, ни осмотические силы. Основной силой, влияющей на свойства СПЭ, был энтропийный фактор, учитывающий число мест, заполненных противоионами. От их соотношения зависит селективность СПЭ и энергия смешения его с раствором. Последняя состоит из трех частей: · энергии Гиббса образования ионных пар между фиксированным ионом и противоионом, которая не является функцией объема, а только числа этих пар; · затем энергии Гиббса, определяемой числом возможных конфигураций матрицы (рассчитывается по теории Флори с двумя допущениями: независимости от заряда матрицы и отсутствия механического натяжения в безводном полиэлектролите); · а также энергии Гиббса распределения ионных пар между активными группами, характеризуемой присоединением каждого противоиона из числа образовавших ионные пары к определенной активной группе.
Последняя составляющая не основывается на цепной модели и зависит от числа ионных пар и объема полиэлектролита.
Экспериментально наблюдается большая сорбция сильных электроли- тов при меньшей обменной емкости СПЭ [12, 13, 23, 29]. Сорбция электроли- тов мала на полностью диссоциированных СПЭ, содержащих, например, сульфогруппы или четвертичные аммониевые основания [13]. Если СПЭ малодиссоциирован или обладает способностью образовывать химические, водородные или другие прочные связи с электролитами (например, карбоксильные СПЭ или аминодиацетатные – Дауэкс А-1), то проникновение сильного электролита в СПЭ растет. Кроме того, если коион обладает большим сродством к СПЭ, то сорбция электролита увеличивается [23, 29].
Поглощение электролита СПЭ зависит также от степени его сшивки: чем она больше, тем меньше концентрация электролита в СПЭ, так как уменьшается его степень набухания [23]. Поглощение электролита зависит от концентрации внешнего раствора. Так при равной концентрации фиксированных ионов, чем больше концентрация электролита, тем больше концентрация внутри зерна приближается к концентрации во внешнем растворе. Причем для малых концентраций равновесного раствора существенную роль играет отношение зарядов коиона к противоиону: чем оно меньше, тем больше концентрация электролита в фазе СПЭ [23, с.30].
Неизвестный коэффициент активности электролита в СПЭ, согласно Доннану, должен мало изменяться при равновесии с разбавленными растворами.
Однако он уменьшается с уменьшением концентрации раствора.
Метод расчета коэффициентов активности соединений противоион – фиксированный ион впервые был рассмотрен в работах Э. Хёгфельда [30] и В. Аргерзингера [31].
Чрезвычайно важный вопрос расчета термодинамических характери- стик СПЭ по данным о распределении растворителя впервые рассматривался Майерсом и Бойдом [32]. Дальнейшее развитие этого направления в работах Г. В. Самсонова с соавт. [33, 34, с.187] позволило получить уравнения для расчета коэффициентов активности компонентов фазы ионита при любых активностях растворителя.
Дэвис и Йомен [13] экспериментально определяли концентрации ионов хлора и водорода в фазах раствора и СПЭ при сорбции соляной кислоты полистирольным СПЭ. Зная средний коэффициент активности электролита во внешнем растворе, они по уравнению Доннана вычисляли средний коэффициент активности электролита в фазе СПЭ. Сравнив полученные величины с табличными для соляной кислоты той же концентрации, что и в фазе СПЭ, они обнаружили разницу в 5% и отнесли ее к сорбции кислоты внутрь СПЭ. Для калиевой формы того же СПЭ поправка должна быть меньше, так как она сорбирует меньше раствора.
Один из вариантов описания и объяснения сверхэквивалентной сорбции состоит в предположении об образовании в системе «необычных» соединений (например, ионных ассоциатов типа HCl2¯ или подобных соединений для серной, фосфорной и др. кислот [35 – 37]). Однако они не дают возможности количественно предсказывать равновесие в системе. Тем не менее, эти работы очень наглядно показывают, что при рассмотрении подобных систем опасно пренебрегать существованием специфических взаимодействий между полиэлектролитом и электролитом, если таковые возможны.
Э. Хёгфельдт [38], занимаясь жидкими экстрагентами с ионообменными свойствами, подтвердил точку зрения Бойда и Линденбаума, что между твердыми и жидкими катионитами существует большое сходство, и показал, что в твердом ионите с 10% сшивки образуются различные комплексы с 1, 2 и 4 молекулами воды. Причем переход к комплексам, обладающим вторичной гидратной оболочкой, совершается скачкообразно. Однако участок, на котором идет формирование первых двух гидратов выбирается произвольно, и, кроме того, значения активности воды на остальных участках определены нечетко. Такой подход позволил ему рассчитать константы и стандартные термодинамические функции образования гидратов в системе при набухании.
По мнению В. С. Солдатова [39 – 41], причина энергетической неоднородности может крыться в том, что большие заряженные фикси- рованные ионы, например, сульфогруппы, из-за стерических затруднений не смогут занять положения, соответствующего наиболее выгодному валентному углу связи (в данном случае, C–S), поэтому в некоторых группах эта связь может оказаться напряженной. Этому может способствовать неравномерное распределение сшивки. Следовательно, разные сульфогруппы могут занимать неравноценные энергетические положения.
В. С. Солдатов и Э. Хёгфельдт [40, 42 – 45] предложили приближенный метод количественного описания зависимостей свойство – состав в ионообменных системах.
Попытки согласовать теорию и практику, не меняя основных предпосылок, предпринимались неоднократно (Грегором, Райсом, а затем Глюкауфом и другими). Наибольшее распространение получил подход, связанный с предположением о неоднородности структуры зерна полиэлектролита. Предполагалось, что полиэлектролит имеет трещины, в которых сорбция происходит по другому механизму, нежели в массе; отдельные включения, селективные к электролиту; неоднородности в распределении ионогенных групп по объему зерна и другие особенности, способные увеличить количество сорбируемого электролита.
Общий итог этих предположений был подведён Глюкауфом в 1962 г.
[46]. Применив оригинальные способ оценки поглощенного электролита, основанный на применении радиоактивных изотопов, и метод расчета поправки на прилипший к поверхности полиэлектролита раствор, авторы получили эмпирическое уравнение, описывающее сорбцию НМЭ в широких пределах концентраций: где AX m – концентрация электролита во внешнем растворе, AX m – концентрация электролита в полиэлектролите, k – константа зависящая от типа электролита, 1 < j < 2.
где AX m – концентрация электролита во внешнем растворе, AX m – концентрация электролита в полиэлектролите, k – константа зависящая от типа электролита, 1 < j < 2.
При этом расчет по теории Доннана предполагает существование приближенной зависимости вида: для электролитов с равновалентными катионом и анионом. Оказалось, что форма уравнения, предложенная Глюкауфом, справедлива в том случае, когда дифференциальная функция распределения функциональных групп по объему имеет совершенно определенный вид:
для электролитов с равновалентными катионом и анионом. Оказалось, что форма уравнения, предложенная Глюкауфом, справедлива в том случае, когда дифференциальная функция распределения функциональных групп по объему имеет совершенно определенный вид: 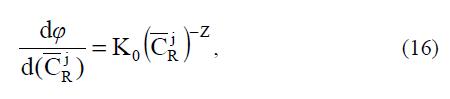 где j R C – концентрация функциональных групп в локальном объеме полиэлектролита; (Cj ) φ R – функция распределения; K0 и Z – константы; 0<Z Отмечены случаи, когда применение уравнений, предложенных Глюкауфом, приводит к неверным выводам о строении СПЭ. В частности, Бутаевым с сотрудниками было обнаружено, что эти уравнения, по крайней мере, в существующем виде, неприменимы, когда наблюдается заметное изменение моляльности функциональных групп от концентрации внешнего раствора [47].
где j R C – концентрация функциональных групп в локальном объеме полиэлектролита; (Cj ) φ R – функция распределения; K0 и Z – константы; 0<Z Отмечены случаи, когда применение уравнений, предложенных Глюкауфом, приводит к неверным выводам о строении СПЭ. В частности, Бутаевым с сотрудниками было обнаружено, что эти уравнения, по крайней мере, в существующем виде, неприменимы, когда наблюдается заметное изменение моляльности функциональных групп от концентрации внешнего раствора [47].
Глюкауфом фактически был оставлен открытым вопрос о свойствах изотермы сверхэквивалентной сорбции для неоднородных полиэлектролитов с иным распределением функциональных групп по объему, отличающимся от выше приведенного. Этот вопрос был подробно проанализирован Ю. А. Кокотовым [48] путем численного решения на ЭВМ уравнения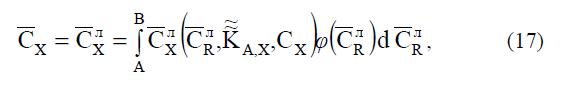 в котором: A,X K ~~ – константа распределения, л R C – концентрация обменных групп в локальном объеме полиэлектролита, л X C – средняя концентрация обменных групп в локальном объеме полиэлектролита для разных вариантов функции ( л ) R φ C и разных значений пределов интегрирования.
в котором: A,X K ~~ – константа распределения, л R C – концентрация обменных групп в локальном объеме полиэлектролита, л X C – средняя концентрация обменных групп в локальном объеме полиэлектролита для разных вариантов функции ( л ) R φ C и разных значений пределов интегрирования.
Автором были проанализированы несколько различных симметричных и несимметричных функций распределения и предложен теоретический аппарат описания исследуемых систем. Им была отмечена сомнительность количественной применимости модели локально – электронейтрального полиэлектролита, суть которой обусловлена наличием в неоднородных полиэлектролитах областей с высокой и низкой локальной концентрацией обменных групп в непосредственной близости друг от друга. По мнению автора, такое соседство должно приводить к образованию заряженного двойного электрического слоя. Наличие таких заряженных областей существенно сказывается на коэффициенте наклона изотермы сорбции.
Несмотря на то, что работы Кокотова существенно проясняют физическую картину взаимодействия СПЭ с растворами НМЭ, практическое применение его результатов затруднено вследствие недостаточных точности и диапазона получаемых изотерм сорбции. Вероятно, поэтому многие ученые ограничиваются при исследовании сорбции подбором коэффициента в уравнении Глюкауфа для данной системы СПЭ – раствор электролита.
В работах А. В. Мамченко и М. С. Новоженюк [49,50] развивается своеобразный подход к проблеме описания равновесия полиэлектролита с раствором. Исходя из общих предпосылок, сходных с теорией Доннана, они получили уравнение изотермы необменной сорбции электролитов в виде: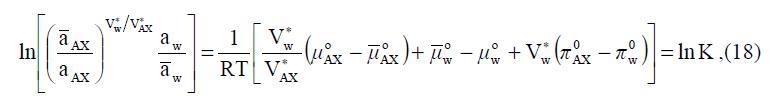 где АХ – электролит; w – вода; Vw * и VАХ * – парциальные мольные объемы воды и электролита; o μi и o μi – химические потенциалы компонентов в стандартных состояниях в фазах раствора и СПЭ; i a и i a – активности компонентов в двух фазах; (p-p0 i) – разность давлений в фазе СПЭ и отсчетной системе для каждого компонента; R – универсальная газовая постоянная; T – температура.
где АХ – электролит; w – вода; Vw * и VАХ * – парциальные мольные объемы воды и электролита; o μi и o μi – химические потенциалы компонентов в стандартных состояниях в фазах раствора и СПЭ; i a и i a – активности компонентов в двух фазах; (p-p0 i) – разность давлений в фазе СПЭ и отсчетной системе для каждого компонента; R – универсальная газовая постоянная; T – температура.
Это уравнение обладает несколько более широкой применимостью, чем уравнения теории Доннана, но при принятых ограничениях (малая необменная сорбция электролита) оно сводится к последним.
Уравнение (18) само по себе не позволяет проанализировать равновесное необменное поглощение электролитов, поскольку включает два неизвестных параметра АХ a и w a . Хотя концентрации двух компонентов (воды и электролита) в фазе СПЭ можно определить экспериментально, необходимы дополнительные уравнения для вычисления активностей или коэффициентов активности каждого компонента в сорбционном растворе.
Связь между величинами i a и i a вытекает из условия равенства химических потенциалов в двух фазах при равновесии в системе: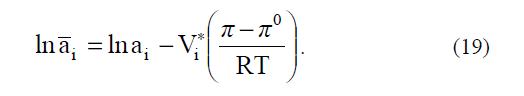 Таким образом, задача вычисления i a сводится авторами к определению разности давлений (p-p0). В связи со сложностью и неточностью обычных методов оценки разности давлений ими была предпринята попытка решить его на основе иного подхода. Они разделили величину — RT 0 π π на две составляющие: — ¥ RT π π и ¥ — RT 0 π π . Здесь p¥ – давление в фазе СПЭ, набухшего в чистом растворителе (воде). Параметр — RT 0 π π при расчетах может оставаться неизвестным, поскольку при вычислениях по соотношению (18) величина, входящая в характеристики каждого из двух компонентов, компенсируется. С учетом этого разложения уравнение (19) примет вид:
Таким образом, задача вычисления i a сводится авторами к определению разности давлений (p-p0). В связи со сложностью и неточностью обычных методов оценки разности давлений ими была предпринята попытка решить его на основе иного подхода. Они разделили величину — RT 0 π π на две составляющие: — ¥ RT π π и ¥ — RT 0 π π . Здесь p¥ – давление в фазе СПЭ, набухшего в чистом растворителе (воде). Параметр — RT 0 π π при расчетах может оставаться неизвестным, поскольку при вычислениях по соотношению (18) величина, входящая в характеристики каждого из двух компонентов, компенсируется. С учетом этого разложения уравнение (19) примет вид: 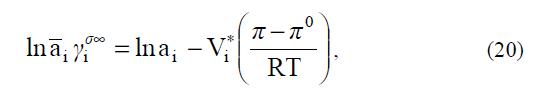 где σ¥ γi = * — RT exp V 0 i π π – коэффициент активности компонента в предельно разбавленном растворе необменно сорбированного электролита.
где σ¥ γi = * — RT exp V 0 i π π – коэффициент активности компонента в предельно разбавленном растворе необменно сорбированного электролита.
Значение второй составляющей давления набухания, зависящей от состава внешнего раствора, может быть вычислено из изотермы необменного поглощения электролита по соотношению: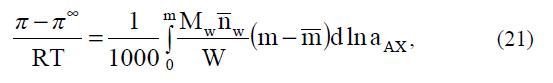 где: m и m – моляльности электролита соответственно в гелевой фазе и во внешнем растворе в условиях равновесия; Mw – мольная масса растворителя (воды); nw – число молей воды поглощенной единицей массы полиэлектролита при моляльности внешнего раствора m; W – объем раствора в гелевой фазе; aАХ – активность электролита во внешнем растворе. Авторам удалось получить неплохое соответствие рассчитанных ими коэффициентов активности и количеств сорбированного электролита с экспериментальными данными.
где: m и m – моляльности электролита соответственно в гелевой фазе и во внешнем растворе в условиях равновесия; Mw – мольная масса растворителя (воды); nw – число молей воды поглощенной единицей массы полиэлектролита при моляльности внешнего раствора m; W – объем раствора в гелевой фазе; aАХ – активность электролита во внешнем растворе. Авторам удалось получить неплохое соответствие рассчитанных ими коэффициентов активности и количеств сорбированного электролита с экспериментальными данными.
В работах Е. М. Кузнецовой [51 – 53] сделана попытка описать сорбцию воды СПЭ с использованием модели сильного электролита, предложенной автором ранее [54]. На основании этой модели было получено выражение для теоретического расчета осмотического коэффициента [55], которое автор применяет для определения разности стандартных значений химических потенциалов в воде и СПЭ ( ow Δμ ). Эта величина (вместе с активностью воды во внешнем растворе) впоследствии используется для того, чтобы найти мольные доли воды в СПЭ. Главный вывод всех указанных работ состоит в том, что ионная форма СПЭ не влияет на величину ow Δμ , которая является функцией диэлектрической проницаемости внутреннего раствора.
Однако вопрос о том, что зерно полиэлектролита не может быть достаточно точно описано с позиции однородного распределения компонентов для большинства исследователей уже не вызывает сомнений [56, гл. 1]. В работе А. Э. Ярощука [57] было показано, что даже если предположить существование гипотетического образца полиэлектролита, не содержащего в своей структуре пор или трещин, намного превышающих размерами дебаевский радиус экранирования, то однородным его можно будет считать только в случае весьма малой удельной емкости. При емкости СПЭ, большей ~ 100 моль/м3 (соответствует достаточно слабым СПЭ), описание зерна СПЭ как гомогенного становится невозможным.
В работах А. Р. Хохлова [58], Т. Танаки [59 – 61], В. Ю. Борю и И. Я. Ерухимовича [62] с позиций теории Флори – Хаггинса и экспериментально было показано, что наличие в набухших СПЭ кулоновских и гидрофобных взаимодействий приводит к богатой картине самоорганизации с образованием упорядоченных микронеоднородностей масштаба 1 – 100 нм.
При изменении качества растворителя(добавление «плохого растворителя», изменении температуры, добавлении НМС) образуется микроструктура с чередующимися гидрофобных незаряженных звеньев и сильнонабухшими областями, в которых находится большинство противоионов. При этом число невыгодных контактов незаряженных звеньев с водой несущественно уменьшается без значительного изменения осмотического давления противоионов. Обравзование микроструктуры возможно уже для геля в набухшем состоянии, что подтверждено экспериментально [59]. То есть наблюдаемое микрофазное расслоение не связано напрямую с коллапсом геля – резким уменьшением макроскопического размера набухших полиэлектролитов с малыми степенями сшивки (до1%) при изменении параметров окружающей среды [62, 63]. Явление коллапса было впервые предсказано К. Душеком [64] и экспериментально обнаружено и детально исследовано Т. Танакой .
Физики, занимающиеся изучением полимеров, рассматривают его как переход клубок – глобула в цепях, составляющих полимерный гель. В результате этого перехода образец геля коллапсирует как целое. Установлено, что с увеличением степени заряженности геля коллапс происходит более резко [63], так как сколлапсированная фаза стабилизируется силами притяжения незаряженных звеньев, и объем геля в этом случае слабо зависит от степени заряженности. Объем же набухшего геля существенно возрастает с ее ростом за счет распирающего осмотического давления противоионов [63, 64].
К представлению структуры набухшего СПЭ как многофазной системы пришли исследователи, занимающиеся изучением состояния иона в СПЭ [65, с. 20-37; 65-69]. Для этого было предложено рассматривать СПЭ как систему пор с заряженными стенками. Причем они могут иметь различную геометрию: плоские, цилиндрические, сферические.
Для получения полуколичественных оценок достаточно рассмотреть плоскую пору. Ю. М. Вольфкович [65,66] использует теорию плоского двойного слоя, а структуру СПЭ моделирует системой пор с заряженными стенками и эффективным радиусом 0,5-100 нм. Средняя поверхностная плотность заряда (σ) оценивается, исходя из предположения о равномерном распределении фиксированных групп по объему СПЭ [65].
Протяженность зоны действия поля индивидуального фиксированного иона, где можно пренебречь влиянием соседних фиксированных ионов, не превосходит 3-6 Ао. В то же время подвижный ион не может приблизиться к фиксированному на расстояние, меньшее суммы радиусов гидратированных ионов, то есть на 6-8 Ао. Заряд фиксированного иона в силу тепловых колебаний размазан по поверхности поры. Поэтому полагают, что электрическое поле плоскости, проходящей через центры противоионов, ближайших к фиксированным ионам, эквивалентно полю, создаваемому равномерно заряженной плоскостью. Таким образом, считают, что заряд диффузной части двойного электрического слоя равен заряду фиксированных ионов, формирующих плоскость с зарядом (σ). Ассоциированные ионы образуют плотную часть двойного слоя. Тогда связь между концентрациями противоионов ( с+ ) и коионов ( с- ) в произвольной точке диффузного слоя имеет тот же вид, что и уравнение (10) при КD=1: Это объясняется тем, что при выводе предполагается идеальность раствора ( 1 i i γ = γ = ); стандартное состояние ионов в диффузном слое – то же, что и в свободном растворе. Таким образом, исключается учет всех видов заимодействий, кроме кулоновских. В уравнении (22) концентрации ионов – локальные, а не усредненные по достаточно большому объему.
Это объясняется тем, что при выводе предполагается идеальность раствора ( 1 i i γ = γ = ); стандартное состояние ионов в диффузном слое – то же, что и в свободном растворе. Таким образом, исключается учет всех видов заимодействий, кроме кулоновских. В уравнении (22) концентрации ионов – локальные, а не усредненные по достаточно большому объему.
Было показано, что соотношение Доннана нельзя применять к большим порам, радиус которых превышает двойную дебаевскую длину экранирования. Внутренняя часть такой поры содержит раствор электронейтрального НМЭ.
Имеется ряд работ [цит. по 65 с.33 – 36], в которых структура СПЭ моделируется системой цилиндрических пор с равномерно заряженными стенками. Распределение электрического потенциала рассчитывается с помощью уравнения Пуассона. Внешняя граница такой «поры» проходит через центры подвижных противоионов, ближайших к фиксированным ионам.
Поверхностная плотность заряда стенок пор рассчитывалась из значений ионообменной емкости.
В работах В. И. Заболоцкого всесторонне рассмотрена микрогетерогенная модель СПЭ [70 – 72]. Набухший СПЭ представляет собой систему, в которой области с относительно равномерным распределением функциональных групп, содержащие воду набухания (структура заряженного геля), соседствуют с электронейтральным раствором, заполняющим внутреннее пространство межгелевых промежутков. К объемным концентрациям противоионов и коионов в гелевой фазе и растворе применимо соотношение Доннана, а концентрации их в каждой из фаз связаны условием электронейтральности. Вводится допущение, что отношение коэффициентов активности электролита в гелевой фазе и в растворе не зависит от концентрации внешнего раствора и, таким образом, коэффициент Доннана (KD) остается постоянным. Отличие от модели Глюкауфа состоит в том, что согласно микрогетерогенной модели концентрация фиксированных ионов в гелевой фазе считается равномерно распределенной, а не изменяющейся от точки к точке.
Микрогетерогенная модель является предельным случаем капиллярной модели бидисперсного СПЭ [23, 56, 66, 73 – 76], если предположить, что в СПЭ существуют мелкие поры, в которых двойные электрические слои перекрываются (гелевая фаза), и крупные поры, радиус которых значительно больше дебаевской длины экранирования (межгелевые промежутки).
В [74, 75] приведены порограммы катионита КУ-2 и анионита АВ-17 и соответствующих мембран на их основе. Видно, что они различаются, прежде всего, наличием второго пика для мембран. По мнению авторов, эти поры (~104 Å) образуются между частицами ионита и полиэтилена. Поры радиусом (15-103 Å) образуют первичную структуру. Она присутствует и в мембранах и в ионитах, хотя в последних объем этих пор существенно меньше. Согласно [76], первичная структура соответствует области гелевых участков и межгелевых промежутков. Гель образуется за счет «связанной» воды, входящей в гидратные оболочки противоионов и в микропоры с радиусом меньше 10 Å.
Гетерогенные модели строения набухшего зерна сшитого полиэлектролита.
Впервые предположение о двухфазном строении зерна СПЭ сделано в работе Девиса и Йомена [13]. Н.П. Гнусин и В.Д. Гребенюк [76] допустили, что в СПЭ имеются гелевые участки, содержащие функ циональные группы, а межгелевые промежутки заполнены равновесным раствором. Это позволило им успешно описать зависимость электропроводности СПЭ от концентрации внешнего раствора. Подобная точка зрения высказывается и в работах Н. П. Березиной о структуре перфторированных мембран [77, 78], состоящих из аморфной кластерной фазы, представляющей совокупность ион – дипольных ассоциатов вблизи боковых сегментов с концевыми сульфогруппами, и фазы, состоящей из воды или раствора электролита, включенной в структурные микрополости полимера.
В рамках подхода к ионообменным мембранам как к двухфазным системам, в работах Н. П. Березиной [77 – 79] рассматриваются перколяцион- ные эффекты в СПЭ (образование проводящих путей в ионообменных материалах в процессе набухания в воде или электролите). Методы теории протекания применялись для описания электрических свойств разных композиционных материалов: полупроводников, сплавов, металлонаполнен- ных полимеров [80]. СПЭ отличаются от них тем, что становятся проводящими лишь в гидратированном состоянии. При набухании в воде или НМЭ ассоциаты зарядов увеличиваются в размерах и сливаются между собой.
Резкое изменение проводимости (критическое влагосодержание) определяется образованием перколяционного бесконечного кластера. Он представляет собой связанную систему гидратированных ионных пар фиксированный ион- противоион. Существуют две возможности образования такого кластера: изменение набухания СПЭ (перколяционные переходы I рода) и варьирование общего количества гидратированных ионных пар фиксированный ион- противоион на стадии синтеза (перколяционные переходы II рода).
При изучении перколяционных переходов II рода расчет объемной доли проводящей фазы проводят, исходя из допущений, что: · вся вода набухания полимерной композиции иммобилизована в составе ион-дипольных ассоциатов фиксированный ион-противоион; совокупность этих ассоциатов представляет собой поликластерную фазу, расположенную между полимерными цепями; · инертная фаза состоит из полимерных цепей, образующих каркас структуры, а также из включений непроводящего термопласта (например, полиэтилена в гетерогенных композициях).
Деление гранулы СПЭ на две фазы для описания СПЭ впервые применил Архангельский [81,82,83 с. 31-41, 84-89]. Одним из основных положений его термодинамических расчетов было то, что граница раздела фаз не отождествляется с видимой границей СПЭ – раствор, а реализуется в объеме СПЭ; то есть, что электролиты А1Xz1 и А2Xz2 практически не смешиваются с z 1 R A 1 и z 2 R A 2 . Таким образом, видимый объем СПЭ и V складывается из объема равновесного раствора p V внутри СПЭ (внутренний раствор) и собственного объема фазы СПЭ R V . Тогда для коэффициента равновесия должно выполняться следующее соотношение: 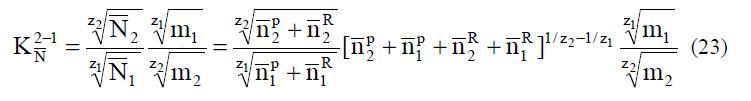 где n – числа молей ионов А1 и А2, N – доля групп, находящихся в ионной форме 1 и в ионной форме 2, а индексы p и R относятся к внутреннему раствору и СПЭ. Если известен объем p V , то есть разность и V − R V , значения p 1 n и p 2 n можно рассчитать по формуле
где n – числа молей ионов А1 и А2, N – доля групп, находящихся в ионной форме 1 и в ионной форме 2, а индексы p и R относятся к внутреннему раствору и СПЭ. Если известен объем p V , то есть разность и V − R V , значения p 1 n и p 2 n можно рассчитать по формуле  где: V – объем равновесного раствора, масса которого равна (1000+m1M1+m2M2), M – молекулярная масса соответствующего электролита, г. Фаза СПЭ представляет собой водный раствор соответствующего мономера (сохраняющего свою форму, имеющего фиксированные ионы и содержащего диспергированную в матрице воду), помещенного в поле действия обобщенных сил (напряжение деформации, напряженность электрического поля, силы поверхностного натяжения).
где: V – объем равновесного раствора, масса которого равна (1000+m1M1+m2M2), M – молекулярная масса соответствующего электролита, г. Фаза СПЭ представляет собой водный раствор соответствующего мономера (сохраняющего свою форму, имеющего фиксированные ионы и содержащего диспергированную в матрице воду), помещенного в поле действия обобщенных сил (напряжение деформации, напряженность электрического поля, силы поверхностного натяжения).
Параметром гетерогенной модели является объем p V , который занимает в СПЭ при активности воды aw необменно поглощенный электролит и вошедшее вместе с ним дополнительное количество воды. Поскольку считается, что СПЭ и поглощенные электролиты не смешиваются, то объем p V равен объему пустот, имеющихся в СПЭ, насыщенном парами воды при активности воды aw. Таким образом, объем R V можно определить в независимом эксперименте и единственным необходимым для расчета параметром является объем и V . Величины R 2 N и R 1 N определяются, если 89 известна емкость СПЭ, то есть число фиксированных ионов R n и коэффициент равновесия 2(R ) 1(R ) N K — , характеризующий распределение противоионов между фазой СПЭ, не содержащей ионов X–, и раствором: 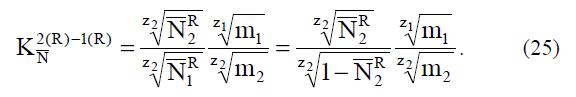 Тогда после расчета величин R 1 n и R 2 n по уравнениям
Тогда после расчета величин R 1 n и R 2 n по уравнениям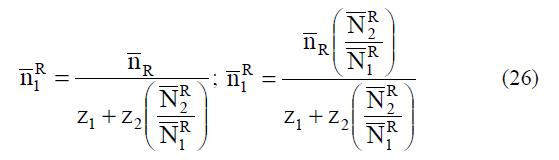 можно, согласно уравнению, (24) определить значение 2(R ) 1(R ) N K — .
можно, согласно уравнению, (24) определить значение 2(R ) 1(R ) N K — .
Архангельский [89] обнаружил, что количество воды, сорбированное одной функциональной группой СПЭ, изменяется в зависимости от активности воды в растворе точно так же, как изотерма сорбции воды для этого СПЭ, снятая изопиестическим методом. Его расчеты совпали с экспериментальными данными для катионитов, но не могли описать взаимодействия анионитов с кислотами.
ЛИТЕРАТУРА.
1. Flory P.J., Rehner J. Statistical mechanics of cross-linked polymer networks. I.Rubberlike elasticity.// J. Chem. Phys. – 1943. – V.11. – P.512-520.
2. Flory P.J. Network structure and the elastic properties of vulcanized rubber.// Chem. Revs. – 1944. – V.35. – P.51-75.
3. Flory P.J. The configuration of real polymer chains.// J. Chem. Phys. – 1949. – V.17. – P.303-310.
4. Flory P.J., Rehner J. Statistical mechanics of cross-linked polymer networks. II.Swelling.// J. Chem. Phys. – 1943. – V.11. – P.521-526.
5. Flory P.J., Fox T.G. Treatment of Intrinsic viscosities.// J. Amer. Chem. Soc. – 1951. – V.73. – P.1904-1908.
6. Flory P.J. Molecular size distribution in three-dimensional polymers.// J. Amer.Chem. Soc. – 1941. – V.63. – P.3083-3100.
7. Flory P.J. Thermodynamics of polymer solutions.// J. Chem. Phys. – 1941. – V.9, № 3. – P.660-664./ Цит. по [89, с.13-27] 8. Flory P.J. Thermodynamics of polymer solutions.// J. Chem. Phys. – 1942. – V.10, № 1. – P.51-53./ Цит. по [89, с.13-27] 9. Flory P.J. Principles of polymer chemistry.// New York: Cornell univ. press. – 1953. – 672 p.
10.Нестеров А.Е., ЛипатовЮ.С. Термодинамика растворов и смесей полимеров.// Киев: Наук. думка, 1984. – 300 с.
11.Huggins M.L. Physical chemistry of polymers.// New York: Intersciens. – 1958. – 175 p./ Цит. по [89, с.13-27].
12.Гельферих Ф. Иониты. Основы ионного обмена.// Пер. с нем. – М.: Изд.ин. лит., 1962. – 490 с.
13.Davies C.W., Yeoman G.D. Swelling equilibria with some cation exchange resins.// Trans. Faraday Soc. – 1953. – V.42, p.8. – P.968-974.
14.Архангельский Л.К.// В кн.: Иониты в химической технологии./ Под ред.Б.П.Никольского, П.Г. Романкова. – Л.: Химия, 1982. – 416 с.
15.Boyd G.E., Soldano B.A. Osmotic Free Energies of Ion-exchangers.Thermodynamic Considaration.// Z. Electrochem. – 1953. – Bd.57, Н.3. – S.162-170.
16.Gregor H.P., Sundheim B.R., Held K.M., Waxman M.H. Studies on ionexchange resins. V. Water vapor sorption.// J. Coll. Sci. – 1952. – V.7, №5. – P.511-533.
17.Gregor H.P., Belle J., Marcus R.A. Studies on ion-exchange resins. IX.Capacity and Specific volumes of quaternary base anion exchange resins.// J.Am. Chem. Soc. – 1954. – V.76, №7. – P.1984-1987.
18.Gregor H.P. Gibbs-Donnan equilibria in ion exchange resin systems.// J. Am.Chem. Soc. – 1951. – V.73, №2. – Р.642-650.
19.Harris F.E., Rice S.A. Model for ion-exchange resins.// J. Chem. Phys. – 1956.– V.24, №6. – P.1258-1264.
20.Bauman W.C., Eichhorn J. Fundamental properties of syntetic cation exchange resin.// J. Am. Chem. Soc. – 1947. – V.69, №11. – P.2830-2836.
21.Donnan F. G., Gugenheim E. A.// Z. Phys. Chem. – 1932. – A162. – Р.346./ Цит. по: Ионный обмен./ Под ред. Я. Маринского. – М.: Мир. – 1968. – С.176-280.
22.Donnan F. G.// Z. Phys. Chem. – 1934. – A168. – Р.369./ Цит. по: Ионный обмен./ Под ред. Я. Маринского. – М.: Мир. – 1968. – С.176-280.
23.КокотовЮ.А., Золотарев П.П., Елькин Г.Е. Теоретические основы ионного обмена: Сложные ионообменные системы.// Л.: Химия, 1986. – 280 с.
24.Glueckauf E., Watts R.E. The Donnan law and its application to ion-exchange polymers.// Proc. Royal Soc., London. – 1962. – V.268, A. – P.339-349.
25.Bauman W.C., Eichhorn J. Fundamental properties of syntetic cation exchange resin.// J. Am. Chem. Soc. – 1947. – V.69, №11. – P.2830-2836.
26.Gregor H.P., Belle J., Marcus R.A. Studies on ion-exchange resins. IX.Capacity and Specific volumes of quaternary base anion exchange resins.// J.Am. Chem. Soc. – 1954. – V.76, №7. – P.1984-1987.
27.Gregor H.P., Sundheim B.R., Held K.M., Waxman M.H. Studies on ionexchange resins. V. Water vapor sorption.// J. Coll. Sci. – 1952. – V.7, №5. – P.511-533.
28.Harris F.E., Rice S.A. Model for ion-exchange resins.// J. Chem. Phys. – 1956.– V.24, №6. – P.1258-1264.
29.Москвичев Б.В., Самсонов Г.В. Необменная сорбция электролитов, содержащих органические ионы.// Журн. физ. химии. – 1968. – Т.40, №1. – С.187-191.
30.Ekedahl E., Högfeld E., Sillen L.G. Activities of the components in ion exchangers.// Acta Chem. Scand. – 1950. – V.4, №3. – Р.556-558.
31.Argersinger W.J., Davidson A.W., jr., Bonner O.D. Thermodynamics and ionexchange phenomena.// Trans. Kansas Acad. Sci. – 1950. – V.53. – P.404-410.
32.Myers G.E., Boyd G.E. A thermodynamic calculation exchange selectivities.// J. Phys. Chem. – 1956. – V.60, №5. – Р.521-529.
33.Самсонов Г.В., Пасечник В.А. Изменение термодинамического потенциала ионообменных смол при ионном обмене.// Журн. физ. химии.– 1962. – Т.36, №12. – С.2727-2733.
34.Самсонов Г.В., Тростянская Е.Б., Елькин Г.Э. Ионный обмен. Сорбция органических веществ.// Л.: Наука, 1969. – 335 с.
35.Полухина Н.А., Шамрицкая И.П., Мирошникова З.П., Хазель М.Ю.Взаимодействие анионита АВ-17 с растворами электролитов.// В сб.: Теория и практика сорбционных процессов. – Воронеж: Изд. ВГУ. – 1972.– Вып. 7. – С.32-37.
36.Муравьев Д.Н. Исследование некоторых особенностей ионного обмена аминокислот и условий противоточной очистки их растворов ионитами.// Дисс… канд. хим. наук. – М., МГУ, 1979.
37.Фесенко С.А. Особенности ионообменных систем включающих кристаллизующиеся в-ва.// Дисс… канд. хим. наук. – М., МГУ, 1983.
38.Хёгфельдт Э. Ионообменная экстракция.// В кн.: Ионный обмен./ Под ред.Я. Маринского. – М.: Мир. – 1968. – С.512-554.
39.Солдатов В.С., Старобинец Г.А. Некоторые вопросы термодинамики катионного обмена.// В сб.: Исследование свойств ионообменных материалов./ Под ред. К.В.Чмутова. – М.: Наука, 1964. – С.36-43.
40.Солдатов В.С. Простые ионообменные равновесия.// Минск: Наука и техника, 1972. – 224 с.
41.Солдатов В.С., Гоголинский В.И., Зеленковский В.М., Пушкарчук А.Л.Влияние структуры узлов сшивки сульфополистирольных катионитов на пространственное размещение сульфогрупп.// Докл. АН Беларуси. – 1996.
– Т.40, №5. – С.65-69, 126.
42.Солдатов В.С., Бычкова В.А. Селективность ионного обмена в неидеальных системах.// Журн. физ. химии. – 1984. – Т.58, №3. – С.665- 668.
43.Kuvaeva Z.I., Soldatov V.S., Fredlund F., Högfeldt E. On the properties of solid and liquid ion exchangers-VI. Application of a simple model to some ion exchange reactions on dinonylnaphtalene sulfonic acid in different solvents and for different cations with heptane as solvent.// J. Inorg. Nucl. Chem. – 1978. – V.40, №1. – P.103-108.
44.Högfeldt E., Soldatov V.S. On the properties of solid and liquid ion exchangers- VII. A simple model for the formation of mixed micelles applied to salts of dinonylnaphtalene sulfonic acid.// J. Inorg. Nucl. Chem. – 1979. – V.41, №4. – P.575-577.
45.Солдатов В.С., Бычкова В.А. Ионообменные равновесия в многокомпонентных системах.// Минск: Наука и техника, 1988. – 360 с.
46.Glueckauf E., Watts R.E. The Donnan law and its application to ion-exchange polymers.// Proc. Royal Soc., London. – 1962. – V.268, A. – P.339-349.
47.Бутаев А.М., Гребень В.П., Тулупов П.Е., Касперович А.И. Необменная сорбция соляной кислоты стиролдивинилбензольными сульфокатионитами.// Журн. физ. химии. – 1973. – Т.47, №7. – С.1817- 1819.
48.КокотовЮ.А. Теория ионного обмена в системах со сверхэквивалентной сорбцией.// Журн. физ. химии. – 1978. – Т.52, №3. – С.672-678.
49.Мамченко А.В., Новоженюк М.С. Расчет необменной сорбции кислот сульфокатионитом в гелеобразной форме.// Химия и технология воды. – 1993. – Т.15, №7-8. – C.508-515.
50.Мамченко А.В., Новоженюк М.С. Коэффициенты активности кислот, необменно сорбированных гелевым сульфокатионитом.// Химия и технол. воды. – 1990. – Т.12, №6. – С.498-505.
51.Кузнецова Е.М., Филиппов О.А. Модель сильного электролита в описании сорбции воды сильнокислотными катионообменниками.// Журн. физ. химии. – 1999. – Т.73, №6. – С.1071-1075.
52.Кузнецова Е.М., Груздева М.А. Модель сильного электролита в описании сорбции воды сильноосновными обменниками.// Журн. физ. химии. – 2000. – Т.74, №6. – С.1136-1138.
53.Кузнецова Е.М. Модель сильного электролита в описании сорбции воды сильнокислотными катионитами в форме многозарядных ионов при 298.15К.// Журн. физ. химии. – 2000. – Т.74, №9. – С.1616-1619.
54.Кузнецова Е.М. Теоретическое описание концентрационного коэффициента активности «сильных» электролитов.// Докл. АН СССР – 1982. – Т.264, №2. – С.360-363.
55.Кузнецова Е.М. Количественное описание термодинамических свойств индивидуальных и смешанных растворов сильных электролитов в различных растворителях и широком интервале концентраций.// Журн. физ. химии. – 1993. – Т.67, №9. – С.1765-1775.
56.Гнусин Н.П., Гребенюк В.Д. Электрохимия гранулированных ионитов. – Киев: Наукова думка, 1972. – 180 с.
57.Ярощук А.Э. О пределах применимости гомогенной модели полиэлектролита в теории ионообменных равновесий.// Журн. физ. химии. – 1986. – Т.60, №4. – С.941-944.
58.Лифшиц И.M., Гросберг A.Ю., Хохлов A.Р. Объемное взаимодействие в статистической физике полимерной макромолекулы.// Успехи физ. наук. – 1979. – Т.127. – С.353-389.
59.Хохлов А.Р., Дормидонтова Е.Е. Самоорганизация в ион-содержащих полимерных системах.// Успехи физ. наук. – 1997. – Т.167, №2. – С.113– 128. (от сих и ниже проверить ссылки на литературу. Возможно эта ссылка не была пронуменована.)
60.Tanaka T. Collapse of gels and the critical endpoint.// Phys. Rev. Lett. – 1978.– V.40, №12. – P.820-823.
61. Shibayama M., Tanaka T., Han C.C.// J. Chem Phys. – 1992. – V.97. – Р.6842./ Цит. по [182].
62.Ohmine I., Tanaka T. Salt effects on the phase transition of ionic gels.// J.Chem. Phys. – 1982. – V.77, №11. – Р.5725-5729.
63.Борю В.Ю., Ерухимович И.Я. Структурные фазовые переходы в растворах слабозаряженных полиэлектролитов. Докл. АН СССР. – 1986. – Т.286, №6.– С.1373-1376.
64.Tanaka T., Fillimore D.J., Sun S.T., Nishiro J., Swislow G., Shah A./Phase transition in ionic gels. // Phys. Rev. Lett. – 1980. – V.45. – P.1636-1639.
65.Dusek K., Prins W.// Adv. Polym. Sci. – 1969. – V.109. – P.1
66. Заболоцкий В.И., Никоненко В.В. Перенос ионов в мембранах.// М.: Наука, 1996. – 392 с.
67.ВольфковичЮ.М., Багоцкий В.С., Сосенкин В.Е., Школьников Е.И. Методы эталонной порометрии и возможные области их применения в электрохимии.// Электрохимия. – 1980. – Т.16, вып. 11. – С.1620-1652.
68.ВольфковичЮ.М., Лужин В.К., Ванюлин А.Н., Школьников Е.И. Применение метода эталонной порометрии для исследования пористой структуры ионообменных мембран.// Там же. – 1984. – Т.20, №5. – С.656- 664.
69.Hopfinger A.J., Mauritz K.A. Theory of the structure of ionomeric membranes.// Comprehensive Theatise of Electrochemistry. Electrochemical Processing. – 1981. – V.2. – P.521-535, цит по [5, гл. 1].
70.Mauritz K.A., Hopfinger A.J. Structural properties of membrane ionomers.// Modern Aspects Electrochem. – 1982. – V.14. – P.425-508, цит. по [5, гл. 1].
71. Заболоцкий В.И., Гнусин Н.П., Шеретова Г.М. Учет структурной неоднородности ионита при описании равновесного распределения электролита в ионообменных системах.// Журн. физ. химии. – 1985. – Т.59, №10. – С.2467-2471.
72. Заболоцкий В.И., Никоненко В.В., Костенко О.Н., Ельникова Л.Ф. Анализ необменной сорбции электролитов ионообменными мембранами с помощью микрогетерогенной модели.// Журн. физ. химии. – 1993. – Т.67, №12. – С.2423-2427.
73.Zabolotsky V.I., Nikonenko V.V. Effect of structural membrane inhomogeneity on transport properties.// J. Membr. Sci. – 1993. – V.79. – P.181-198.
74.КокотовЮ.А. О влиянии неоднородности полиэлектролита на изменение сорбции необменно-поглощенного электролита.// Журн. физ. химии. – 1978. – Т.52, №1. – С.178–182.
75.Березина Н.П., ВольфковичЮ.М., Кононенко Н.А., Блинов Н.А. Изучение распределения воды в гетерогенных ионообменных мембранах методом эталонной порометрии.// Электрохимия. – 1987. – Т.23, вып. 7. – С.912- 916.
76.Кононенко Н.А., Березина Н.П., ВольфковичЮ.М., Школьников Е.И., Блинов Н.А. Исследование структуры ионообменных материалов методом эталонной порометрии.// Журн. прикл. химии – 1985. – №10. – С. 2199- 2203.
77.Гнусин Н.П., Гребенюк В.Д., Певницкая М.В. Электрохимия ионитов. – Новосибирск: Наука, Cибирское отд., 1972. – 200 с.
78.Березина Н.П., Гнусин Н.П., Демина О.А. Модельное описание электротранспорта воды в ионообменных мембранах.// Электрохимия. – 1990. – Т.26, вып. 9. – С.1098-1104.
79.Березина Н.П., Тимофеев С.В., Демина О.А., Озерин А.Н., Ребров А.В. Комплексное исследование электротранспортных свойств перфторированных мембран с различной влагоемкостью.// Электрохимия. – 1992. – Т.28, вып. 7. – С.1050-1058.
80.Березина Н.П., Карпенко Л.В. Перколяционные эффекты в ионообменных материалах.// Коллоидн. журн. – 2000. – Т.62, № 6. – С.1-9.
81.Шкловский Б.И., Эфрос А.Л. Теория протекания и проводимость сильно неоднородных сред.// Успехи физ. наук. – 1975. – Т.117, вып.3. – С.401- 434.
82.Архангельский Л.К., Воеводина А.А., Матерова Е.А. Взамодействие ионообменных смол с водой.// Вестник ЛГУ. Сер. физ. и хим. – 1961. – №22, вып.4. – С.102-110.
83.Архангельский Л.К., Матерова Е.А. О некоторых закономерностях поглощения паров воды смешанными формами сульфокатионитов с различным числом поперечных связей.// Вестник ЛГУ. – 1968. – №10, вып. 2. – С.146-148.
84.Архангельский Л.К.// В кн.: Иониты в химической технологии./ Под ред. Б.П.Никольского, П.Г. Романкова. – Л.: Химия, 1982. – 416 с.
85.Tye F.L. Absorption of electrolytes by ion-exchange materials.// J. Chem. Soc. – 1961. – P.4784-4789.
86. Juda W., Rosenberg N.W., Marinsky J.A., Kasper A.A. Electrochemical properties of ion exchane rasins. I. Donnan Equilibria, membrane potentials and conductivities.// J. Am. Chem. Soc. – 1952. – V.74, №15. – P.3736-3738.
87. Freeman D.H. Electrolyte uptake by ion-exchange resins.// J. Phys. Chem. – 1960. – V.64, №8. – Р.1048-1051.
88.Матерова Е.А., Рожанская Т.И., Сирота З.М. Электрохимические свойства мембран из анионитов, отличающихся структурой ионогенной группы. I. Необменное поглощение электролитов мембранами.// Электрохимия. – 1965. – Т.1, вып.7. – С.794-799.
89.Мелешко В.П., Шамрицкая И.П., Полухина Н.А., Селеменев В.Ф. Об особенностях сорбции серной кислоты на высокоосновных анионитах.// Журн. физ. химии. – 1970. – Т.44, №7. – С.1748-1751.
90.Архангельский Л.К., Матерова Е.А., Кисельгоф Г.В. Изучение ионообменного равновесия. Обмен ионов на сульфокатионитах с разным содержанием дивинилбензола.// Вестн. ЛГУ. – 1965. – №16. – С.74-82.

