Физическая химия полимерных гелей Лекция 21 ВЛИЯНИЕ РАЗМЕРА ГРАНУЛ И КОНЦЕНТРАЦИИ РАСТВОРА KCL НА КИНЕТИКУ НАБУХАНИЯ ИОНИТОВ: КУ-2Х4, КУ-2Х8, АРА4П И АВ- 17Х8

Физическая химия полимерных гелей Лекция 20 ГЕТЕРОФАЗНАЯ ФИЗИКО-МАТЕМАТИЧЕСКАЯ КИНЕТИЧЕСКАЯ МОДЕЛЬ НАБУХАНИЯ ПОЛИМЕРНЫХ ГЕЛЕЙ
19.12.2015
Физическая химия полимерных гелей Лекция 22 ВЛИЯНИЕ ПРИРОДЫ И КОНЦЕНТРАЦИИ РАСТВОРЕННОГО ВЕЩЕСТВА НА КИНЕТИКУ НАБУХАНИЯ СУЛЬФОКАТИОНИТОВ НА ОСНОВЕ СШИТОГО ПОЛИСТИРОЛА
19.12.2015Физическая химия полимерных гелей Лекция 21 ВЛИЯНИЕ РАЗМЕРА ГРАНУЛ И КОНЦЕНТРАЦИИ РАСТВОРА KCL НА КИНЕТИКУ НАБУХАНИЯ ИОНИТОВ: КУ-2Х4, КУ-2Х8, АРА4П И АВ- 17Х8
Физическая химия полимерных гелей
Ферапонтов Н. Б., Гагарин А. Н., Струсовская Н. Л., Токмачёв М. Г., Тробов Х.Т., Рубин Ф.Ф.
Москва, МГУ имени М. В. Ломоносова 2015 г.
Для проверки адекватности описания кинетической моделью получаемых экспериментальных результатов, исследуем с ее помощью кинетику набухания нескольких полимеров. На первом этапе проанализируем влияние размера гранул полимера и концентрации внешнего раствора на кинетику набухания полиэлектролитов на основе полистирола, сшитого дивинилбензолом: КУ-2х4 и КУ-2х8 в К-форме, а также АРА-4П и АВ-17х8 в С1-форме в растворах КС1 разной концентрации. Имея одинаковую матрицу, указанные полимеры различаются природой полярных групп и количеством сшивки. Выбор КС1 основан на том, что этот электролит наиболее индифферентен к полимерам, т.е. не взаимодействует с ними и не проникает в фазу ПР.
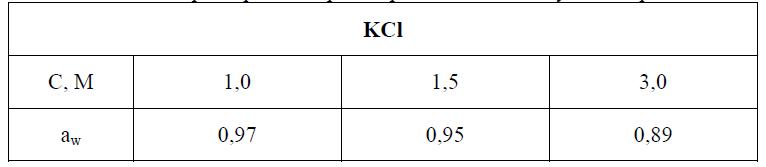
Проанализируем кинетику набухания данных ионитов на гранулах трех размеров: «больших» (диаметром 0,89-0,99 мм); «средних» (диаметром – 0,60-0,73 мм) и «малых» (диаметром – 0,36-0,49 мм). Указанные размеры, это диаметры гранул, набухших в воде. Кинетику набухания изучали в растворах KCl ( табл. 1).
Таблица 1. Характеристики растворов КС1, используемых в работе.
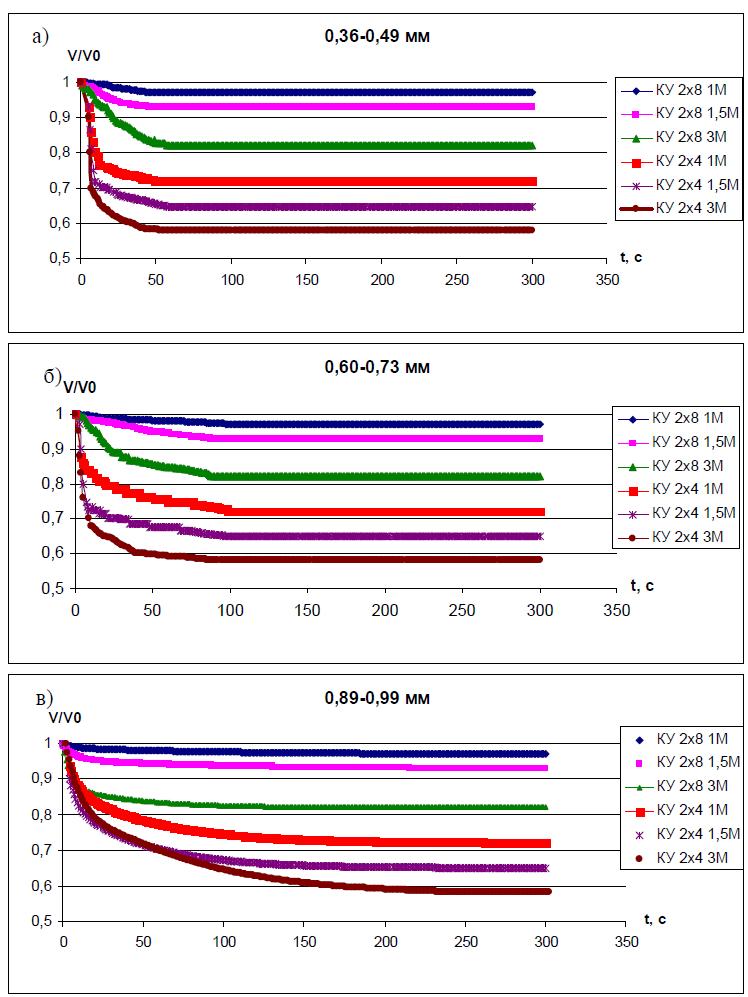
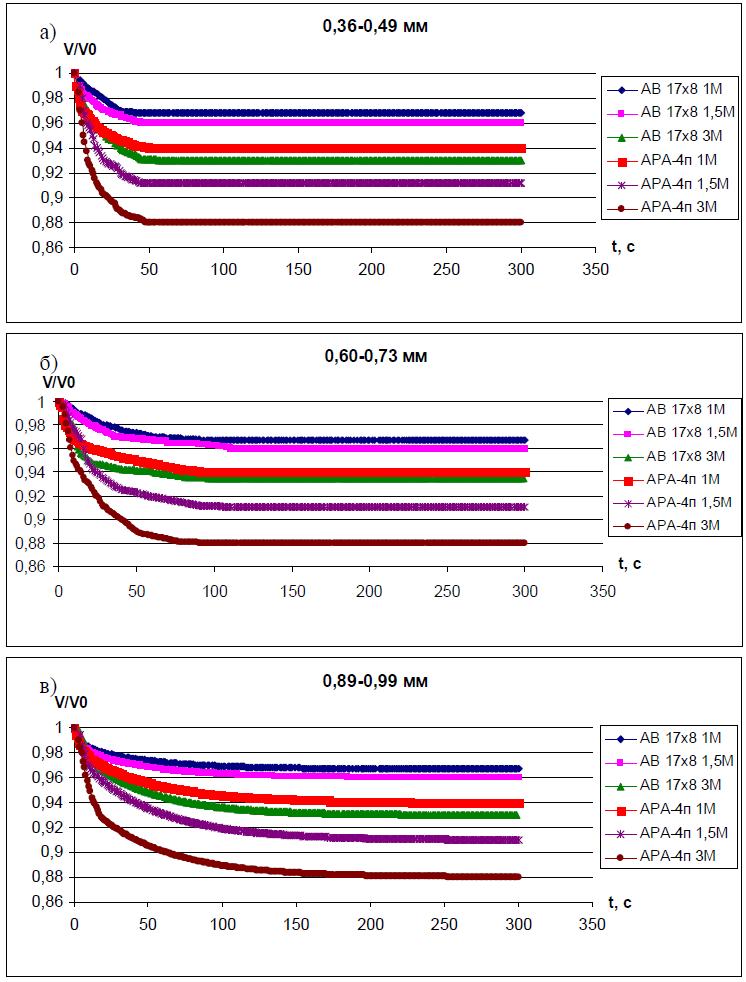
Ниже на рис. 1 и 2 представлены результаты экспериментов, иллюстрирующие изменение во времени относительного объёма гранул разного размера в растворах КС1 разной концентрации.
Рис. 1. Кинетика набухания К-формы катионитов КУ-2х4 и КУ-2х8 в зависимости от концентрации раствора КС1 и размера гранул.
Рис. 2. Кинетика набухания гранул анионитов АРА-4П и АВ-17х8 в С1-форме в зависимости от концентрации раствора КС1 и размера гранул.
Как видно из полученных результатов изменение степени набухания всех исследованных полимеров в растворах КС1 имеет разную, но достаточно простую кинетическую зависимость. Кроме того, из анализа приведенных графиков следует, что все исследованные полиэлектролиты обладают следующими свойствами:
1. В растворах КС1 одинаковой концентрации время выхода на равновесие тем меньше, чем меньше размер гранулы. При этом размер гранулы не влияет на значение равновесного относительного объёма.
2. При увеличении концентрации раствора, величина равновесного относительного объёма уменьшается. При этом время выхода на равновесие (для гранул одного размера) практически не меняется.
3. Значения равновесных относительных объёмов в растворах одной и той же концентрации больше для полиэлектролитов с большим количеством сшивки. То есть изменение степени набухания полимера уменьшается с увеличением количества сшивки. При этом время выхода на равновесие практически не меняется.
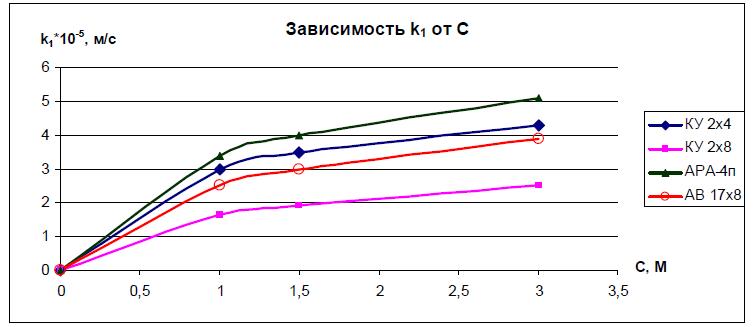
По полученным экспериментальным результатам для этих четырёх исследованных ионитов были определены коэффициенты модели: k1, k2 и k3 (см. лекцию 24). Результаты расчетов представлены на рис. 3-7.
Рис. 3. Зависимость коэффициента k1 от концентрации раствора КС1.
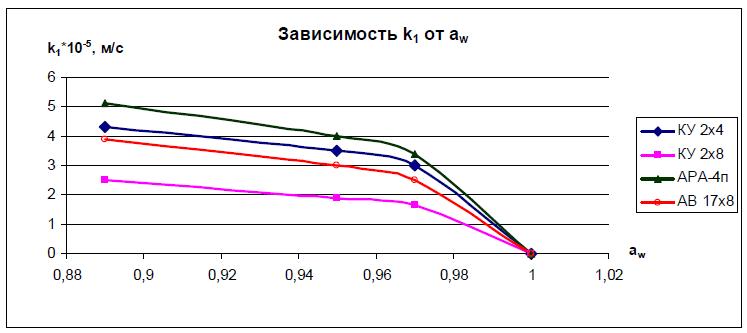
Рис. 4. Зависимость коэффициента k1 от активности воды в растворе КС1.
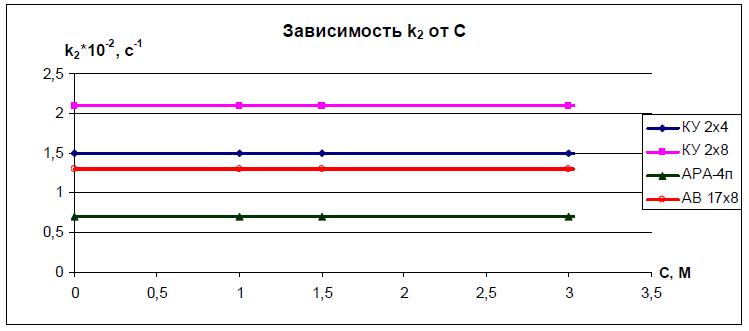
Рис. 5. Зависимость коэффициента k2 от концентрации раствора КС1.
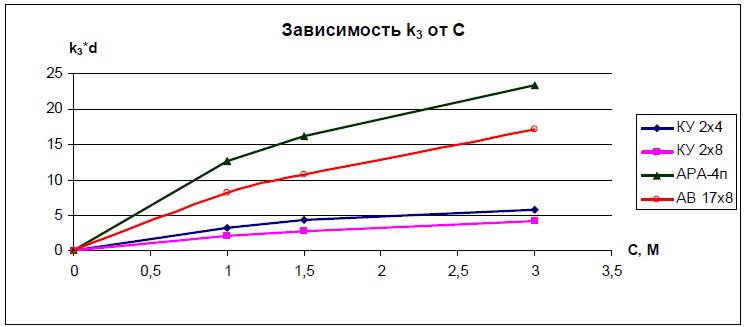
Рис. 6. Зависимость произведения k3·d от концентрации раствора КС1.
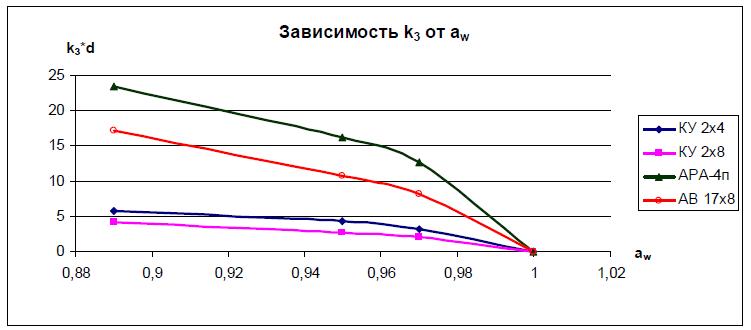
Рис. 7. Зависимость произведения k3·d от активности воды в растворах КС1.
Из данных, представленных на рисунках 3-7 следует, что:
1. В исследованном интервале размеров гранул их диаметр не влияет на коэффициенты k1 и k2.
2. Коэффициент k3 увеличивается с уменьшением диаметра гранулы. При этом установлено, что в пределах одной концентрации произведение k3*d = k3 отн. остаётся постоянным (d – диаметр гранулы в воде).
3. С ростом концентрации, коэффициенты k1 и k3 увеличиваются, а k2 от концентрации не зависит.
4. С увеличением количества сшивающего агента, увеличивается коэффициент k2, но уменьшаются k1 и k3.
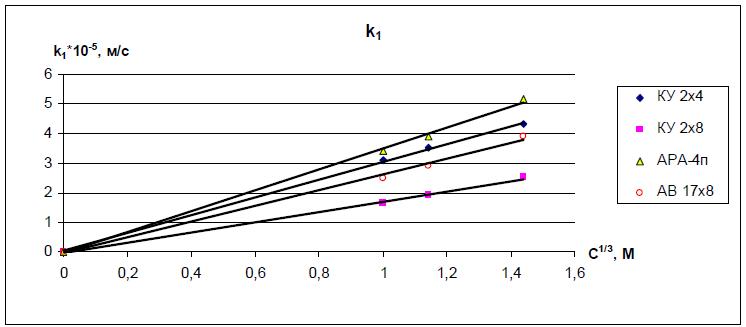
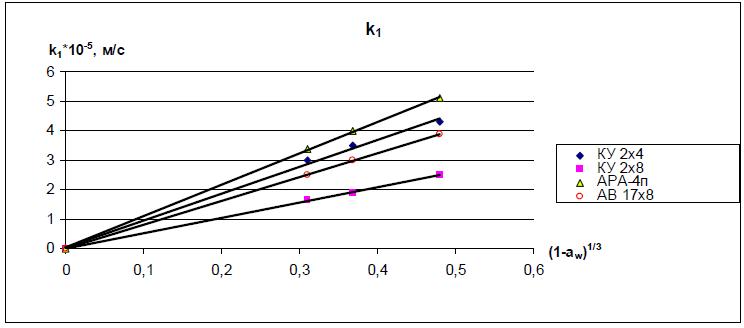
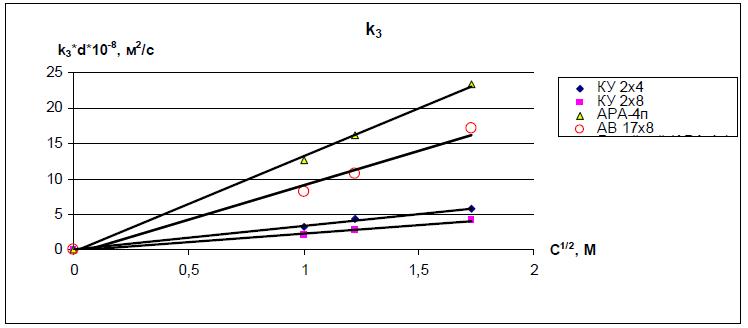
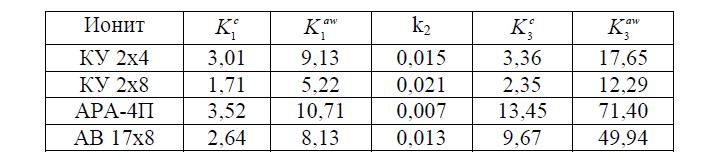
Последующий анализ полученных результатов показал, что k1 линейно зависит от кубического корня из концентрации или активности воды (1-aw), то есть k1 = c K1 ·C1/3 или k1 = aw K1 ·(1-aw)1/3. Коэффициент k3 линейно зависит от квадратного корня из концентрации или от активности воды (1-aw), т.е. k3 отн. = c K3 ·С1/2 или k3 отн. = aw K3 ·(1-aw)1/2. Полученные зависимости, а также найденные значения больших коэффициентов К1 и К3 приведены в рис. 8 – 11 и таблице 2. Кроме того, результаты экспериментов показали полное соответствие значений коэффициентов, полученных в «прямых» и в «обратных» экспериментах.
Рис. 8. Зависимость коэффициента k1 от кубического корня из концентрации.
Рис. 9. Зависимость коэффициента k1 от кубического корня из (1-aw).
Рис. 10. Зависимость произведения k3·d от квадратного корня из концентрации.
Рис. 11. Зависимость произведения k3·d от квадратного корня из (1-aw).
Таблица 2. Значения коэффициентов К1, k2 и K3, полученные для К-формы и С1-формы ионитов.
Представленные результаты позволяют сделать следующие выводы:
1. Исследованная модель достаточно подробно описывает экспериментальные кинетические зависимости.
2. Для каждого из указанных ионитов значения коэффициентов К1, k2 и K3 являются постоянными и могут быть использованы для априорного описания кинетики его набухания в растворах КС1 любых концентраций.