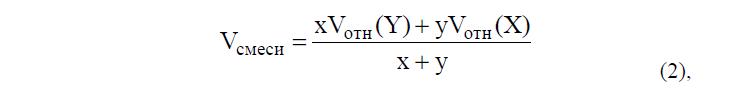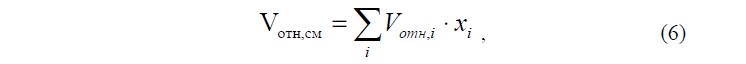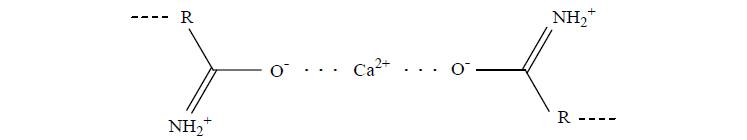Физическая химия полимерных гелей Лекция 33 НЕКОТОРЫЕ АНАЛИТИЧЕСКИЕ СВОЙСТВА ПОЛИМЕРНЫХ ГЕЛЕЙ
Физическая химия полимерных гелей Лекция 33 НЕКОТОРЫЕ АНАЛИТИЧЕСКИЕ СВОЙСТВА ПОЛИМЕРНЫХ ГЕЛЕЙ
Физическая химия полимерных гелей
Ферапонтов Н. Б., Гагарин А. Н., Струсовская Н. Л., Токмачёв М. Г.
Москва, МГУ имени М. В. Ломоносова 2015 г.
1. Оптический метод определения природы и концентраций растворенных веществ.
В работе [1] для определения природы и концентрации растворенных веществ в качестве чувствительного элемента предложено использовать иониты. Однако, сшитые гидрогели, представителями которых являются сшитые ПВС и ПААм, более удобны для определения концентраций растворенных веществ, так как их полярные группы не вступают во взаимодействие с растворенным веществом, а степень набухания таких гелей сильно и адекватно зависит от состава раствора [2, 3].
Свойство ПВС: заметно изменять степень набухания в зависимости от свойств внешнего раствора, было эффективно реализовано в аналитическом методе определения состава раствора, где гранулы ПВС используются как датчики [4, 5]. В этом методе концентрация вещества определяется как функция размера гранулы, поэтому, чем больше изменение объема, тем выше чувствительность метода. При изучении возможности определения концентраций растворенных веществ в растворах смесей установлено, что степень набухания геля ПВС зависит от доли каждого из компонентов смеси в анализируемом растворе. При этом набухание пропорционально долям растворенных НМС. Данный результат позволяет использовать для определения концентраций веществ в растворах смесей базу данных о набухании геля ПВС в бинарных растворах, что значительно упрощает анализ.
Еще одно достоинство метода состоит в том, что с его помощью можно анализировать растворы любого состава. Это касается не только природы растворенного вещества, но и природы растворителя [6, 7]. Сшитый ПВС является удобным сенсором, так как степень его набухания в растворах веществ разной природы и концентрации сильно различается. Это свойство ПВС обеспечивает достаточно высокую точность измерений. Еще одним важным достоинством метода является возможность уменьшения объема пробы. Если диаметр гранулы уменьшить до 10мкм, то объем пробы уменьшится до десятых долей микролитра.
2. Алгоритм расчета состава раствора смеси из двух низкомолекулярных соединений.
При теоретическом расчете относительного объема гранулы в растворе смеси веществ X и Y с соотношением x:y сначала вычитают из объема гранулы в бинарном растворе вещества X объем гранулы в бинарном растворе вещества Y:
Разделив эту разность на x+y частей, записывают уравнение для вычисления относительного объема гранулы полимера в растворе смеси:
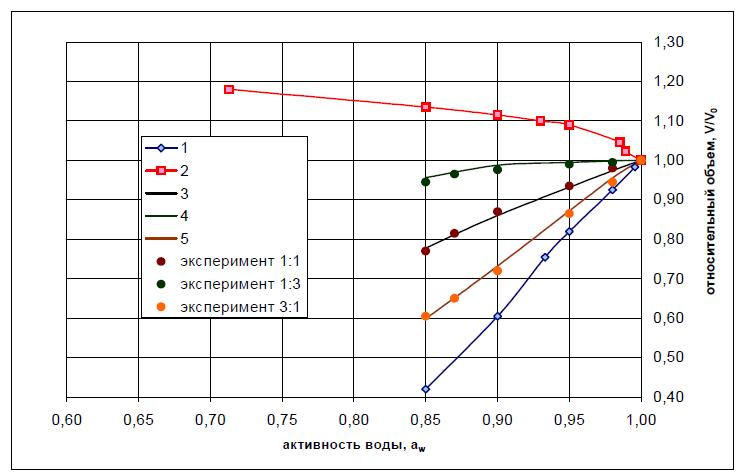
, где x и y – объемные доли X и Y в смеси, а Vотн(X) и Vотн(Y) – относительные объемы гранулы в бинарных растворах X и Y соответственно. Задавая различ- ные соотношения величин х и у, получают набор кривых, показывающих изменение объема гранулы в зависимости от суммарной концентрации раство- ра и доли каждого из компонентов. В качестве примера на рис. 1 и 2 приведено сравнение результатов, полученных расчетом и в результате непосредствен- ных экспериментальных измерений. На них показано, как изменяется относительный объем гранулы ПВС в растворах разного состава для смеси соляной кислоты и хлорида калия, а также для смеси серной и соляной кислот.
Точками на рисунках показаны экспериментально определенные объемы, а линиями – относительные объемы, вычисленные по уравнению (2). Видно, что результаты расчета и эксперимента совпадают. Такое же соответствие наблюдается и для всех остальных исследованных систем.
Однако, чтобы определить индивидуальные концентрации растворен- ных веществ, кроме степени набухания необходимо знать и активность воды x y xV (Y) yV (X) V отн отн смеси + = + в анализируемом растворе. Ее находят с учетом природы анализируемых веществ, используя другие сшитые полимеры (чаще иониты).
Рис. 1. Влияние природы и концентрации растворенных веществ на набухание геля ПВС-20: 1 – в растворах KCl; 2 – в растворах HCl; 3 – в растворах смеси HCl–KCl в соотношении 1:1; 4 – в растворах смеси HCl–KCl в соотношении 1:3; 5 – в растворах смеси HCl–KCl в соотношении 3:1.
Если активность воды и степень набухания ПВС в анализируемом растворе определены, то его состав также можно считать определенным, так как координатам найденной точки соответствует только один состав анализируемого раствора.
С помощью оптического метода можно анализировать растворы и более сложного состава, однако если анализируемый раствор содержит более двух растворенных веществ, то для определения концентраций в таких смесях необходимо использовать либо разбавление исследуемого раствора в известное число раз, либо использовать дополнительные сорбенты с другими характеристиками относительных объемов.
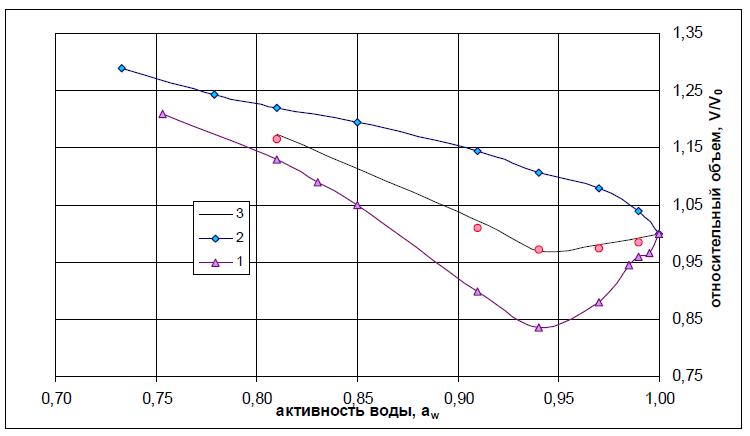
Рис. 2. Влияние природы и концентрации раствора на набухание ПВС-20: 1 – в растворах H2SO4; 2 – в растворах HCl; 3 – в растворах смеси H2SO4-HCl в соотношении 1:1.
Приведенные результаты позволяют говорить о том, что предлагаемый метод является достаточно удобным и эффективным, а использование в нем ПВС значительно расширяет круг решаемых аналитических задач.
3. Определение концентраций веществ в многокомпонентных смесях
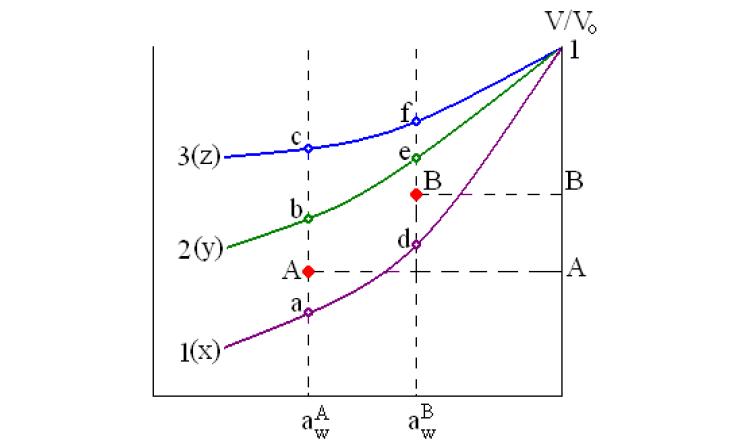
Гранулы ПВС могут быть использованы и для анализа растворов более сложного состава. Также как и для систем, содержащих два растворенных вещества, для определения концентраций веществ в более сложных смесях, необходимо в базе данных прибора иметь информацию о влиянии активности воды на степень набухания геля ПВС в бинарных растворах веществ, присутствующих в анализируемой смеси. Кроме того, должен быть подобран сорбент, позволяющий установить активность воды в анализируемом растворе. После того, как активность воды установлена, проводят измерение относительного объема гранулы ПВС в анализируемом растворе. Пусть эта величина соответствует координате точки А (см. рис. 3). На этом рисунке приведены три кривые: 1, 2 и 3, которые изображают три индивидуальные зависимости для трех растворенных веществ.
Рис. 3. Схема определения концентраций веществ в трехкомпонентной смеси (1, 2 и 3 – индивидуальные зависимости для растворенных веществ; x, y и z – доли этих компонентов в смеси; a, b, c – величины относительного объема гранулы полимера при A aw ; d, e и f – величины относительного объема гранулы полимера при B aw ).
Пусть x, y и z – доли этих веществ в анализируемом растворе. Тогда для решения нашей задачи можно записать:
x + y + z =1 (3)
то есть сумма долей компонентов смеси рана единице.
Если координаты точки А известны, то можно записать уравнение (4):
a* x + b * y + c * z = A (4)
где: a, b и c – известные величины, показывающие значение относительного объема для бинарных растворов компонентов смеси при активности воды в растворе, равной A a w .
Если анализируемая смесь состоит из трех компонентов, то необходимо провести еще одно измерение относительного объема, но при другой активности воды. Наиболее просто это сделать, воспользовавшись разведением анализируемого раствора в известное число раз. Таким образом получают точку В (см. рис. 3). Зная ее координаты, записывают уравнение (5):
d * x + e * y + f * z = B (5)
где: d, e и f – известные величины, показывающие значение относительного объема для бинарных растворов компонентов смеси при активности воды в растворе, равной В a w .
Таким образом, мы получили три уравнения с тремя неизвестными.
Решив эту систему, находим интересующие нас величины. Понятно, что, используя данный прием можно анализировать и более сложные смеси.
4. Взаимодействие геля поливинилового спирта с растворами низкомолекулярных соединений.
Среди поставленных в работе задач наибольший интерес, вероятно, вызывает ответ на вопрос о влиянии природы и концентрации растворенных веществ на состав геля полимера. Оптическим методом были проведены измерения объемов гранул ПВС, набухших в растворах известных составов.
По результатам этих измерений был получен набор зависимостей, иллюстрирующих изменение относительного объема геля от концентрации растворенного вещества. Показано как степень набухания геля полимера в водных растворах НМС зависит от концентрации растворенного вещества и от его природы. При этом растворенное вещество не образовывало с полимером новых соединений, и, следовательно, изменение степени набухания происходило в результате разрыва или образования водородных связей между водой, полимером и растворенным веществом. Количество и энергия таких связей зависят от природы растворенного вещества и его концентрации, что и наблюдалось при проведении экспериментов.
Полученные результаты показали, что на объем геля влияет природа как катиона так и аниона Как было показано в работе [8], в ряду катионов степень набухания полимера уменьшается с увеличением ионного радиуса катиона. В работе [2] показано, что в случае анионов картина меняется: увеличение радиуса аниона приводит к увеличению степени набухания геля.
Кроме того, установлено, что при замене противоиона последовательности в рядах набухания, как катионов, так и анионов, сохраняются. Это говорит о том, что образующаяся между полимером и каждым из ионов НМС связь носит самостоятельный, индивидуальный характер. То есть на набухание полимера оказывает влияние природа обоих ионов, но в эксперименте виден результат только их совокупного влияния.
Кроме ионного радиуса и знака заряда, на степень набухания геля оказывает влияние и величина заряда иона. Например, ионные радиусы иона натрия (0,98 A) и кальция (1,04 A) мало различаются, но степень набухания их галогенидов различается сильно.
Как известно наиболее эффективно разрушает водородные связи между полимерными цепями ион водорода, поэтому в растворах кислот гель ПВС набухает особенно сильно. Однако в растворах кислот на степень набухания полимера кроме протона оказывает влияние и природа аниона. Как показали опыты с растворами сульфата натрия, присутствие сульфат-иона в растворе приводит к значительному уменьшению объема геля. Очевидно, что причина связана с природой этого иона. В работе [9], говорится о том, что атомы кислорода сульфат-иона легко образуют прочные водородные связи с полярными группами органических молекул, в том числе и ROH-группами. В данном случае это приводит к образованию дополнительных сшивок между полимерными цепями и, соответственно, снижению степени набухания геля.
Прочность этих связей настолько велика, что влияние сульфат-иона проявляется даже в растворах серной кислоты.
Следует обратить внимание и на другой результат, характеризующий влияние природы ионов на набухание геля ПВС. Он касается растворов двух НМС: соляной кислоты и иодида натрия. Полученные оптическим методом зависимости относительного объема геля от концентрации раствора очень похожи, хотя природа и катиона и аниона различны. Если в случае соляной кислоты разрушителем водородных связей является протон, то в растворах иодида натрия эту функцию выполняет иодид-ион. Разрушительные свойства иодид-иона оказались настолько велики, что в концентрированных растворах иодида кальция приводят к разрушению гранул геля.
Анализируя результаты, полученные оптическим методом, следует обратить внимание на оригинальные формы зависимости величины степени набухания геля, от природы и концентрации растворенного вещества. Среди исследованных НМС нет таких, набухание в растворах которых совпадало бы с набуханием в растворе другого НМС. Именно это свойство геля ПВС позволяет определять природу растворенного вещества, а если природа известна, то его концентрацию.
4.1 Анализ природных вод.
В поиске решения практической задачи, заключающейся в определении концентраций компонентов в смешанных растворах, было проанализировано поведение ряда полимеров в растворах некоторых двухкомпонентных смесей. Сорбенты для анализа смесей выбирались таким образом, чтобы на выбранном сорбенте зависимости изменения Vотн от концентрации для индивидуальных компонентов этой смеси имели сильно различающуюся область. Было проанализировано поведение ПАА-2%-р в растворе, содержащем хлориды натрия и кальция, а также в растворе смеси сульфата и хлорида натрия. Было проведено несколько измерений с использованием ПВС-20 для проверки справедливости проведения расчетов, основанных на уравнении (5) в области малых концентраций. Ранее этот сорбент уже показал своюприменимость для анализа смесей в растворах более высоких концентраций.
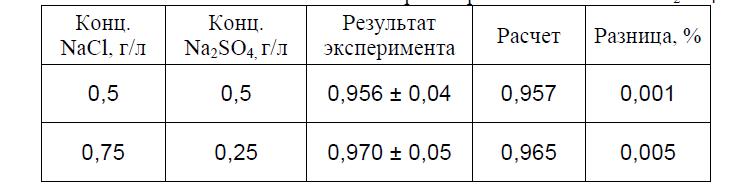
В таблице 1. приведены экспериментальные и расчетные значения относительного объема геля ПВС-20 в растворах смесей хлорида и сульфата натрия указанных концентраций, из которых также следует, что ПВС-20 изменяет свой объем в соответствии с уравнением (5).
Таблица 1. Сравнение экспериментальных и рассчетрных значений относительного объема геля ПВС-20 в растворах смесей NaCl и Na2SO4.
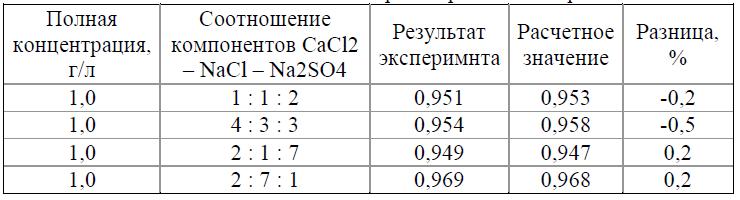
 С практической точки зрения большой интерес представляет поведение гидрогелей в растворах смесей тех НМС, которые в основном присутствуют в пресных природных водах. Соответствующие эксперименты были проведены с гелем ПВС-20. Результаты экспериментов и расчетов приведены в таблице 2. Видно, что экспериментально полученные значения хорошо описываются уравнением (6).
С практической точки зрения большой интерес представляет поведение гидрогелей в растворах смесей тех НМС, которые в основном присутствуют в пресных природных водах. Соответствующие эксперименты были проведены с гелем ПВС-20. Результаты экспериментов и расчетов приведены в таблице 2. Видно, что экспериментально полученные значения хорошо описываются уравнением (6).
где Vотн,см – относительный объем геля в растворе смеси нескольких компонентов при определенной активностью воды (aw), xi – доля i-го компонента в растворе, Vотн,i – известные величины, показывающие значение относительного объема для бинарных растворов i-х компонентов смеси при активности воды в растворе, равной aw.
Очевидно, что корректнее было бы изучать изменение объема геля в зависимости от активности воды в растворах смесей, однако в области таких низких концентраций активность воды практически равна единице. Это заставило изучать влияние концентрации растворенных веществ на степень набухания геля в зависимости от суммарной концентрации растворенных веществ в растворе.
При проведении экспериментов было установлено, что недостатком гидрогеля ПВС-20, в применении к анализу разбавленных смешанных растворов, является тот факт, что заметное различие в степени набухания геля наблюдается только в области концентраций, превышающих 0,8 г/л, где становится заметным достаточно резкое уменьшение относительного объема геля в растворах.
Таблица 2. Сравнение экспериментальных и расчетных значений относительных объемов геля ПВС-20 в растворах смесей трех компонентов.
5. Использование ПААм в качестве чувствительного элемента в методе оптической микрометрии.
Одним из гидрогелей, применяемых в МОМ, является полиакриламид.
В зависимости от условий полимеризации поведение геля ПААм в растворах заметно различается. Влияние сшивки можно наблюдать на рис. 4. Видно, что при увеличении степени сшивки изменение объема геля при идентичных внешних условиях становится менее значительным, поэтому особенно заметным оказалось влияние концентрации раствора на степень набухания ПААм-2%-р.
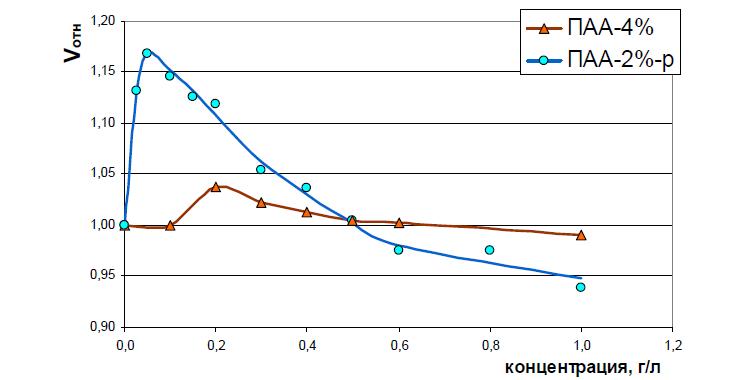 Рис. 4. Сравнение зависимостей относительных объемов геля ПААм от концентрации раствора NaHCO3 для ПАА-2%-р и ПААм-4%.
Рис. 4. Сравнение зависимостей относительных объемов геля ПААм от концентрации раствора NaHCO3 для ПАА-2%-р и ПААм-4%.
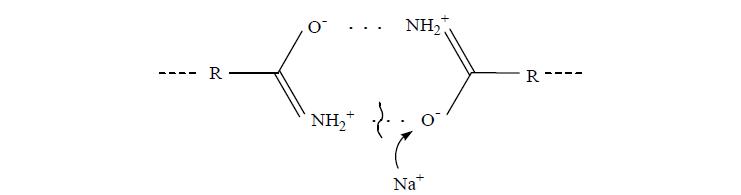
В отличие от других сорбентов, относительный объем ПААм-2%-р претерпевает существенное изменение в зависимости от природы и концентрации солей в области низких концентраций (до 0,2 г/л). Причина состоит в том, что мезомерное строение полиакриламида допускает образование водородных связей между функциональными группами, принадлежащими различным участкам полимерной цепи. Присутствие даже небольших количеств катионов натрия приводит к разрыву водородных связей, что и проявляется в виде скачкообразного увеличения относительного объема геля. Атака кислорода амидной группы катионом натрия, присутствующим в растворе, с последующим разрушением водородной связи, схематически изображена на рис. 5 При дальнейшем увеличении концентрации растворов относительный объем геля начинает снижаться, что возможно связано с уменьшением числа молекул воды в фазе ПР.
Рис. 5. Разрушение катионом натрия водородных связей в структуре ПААм.
В отличие от катиона натрия, катион кальция, являясь двухвалентным, способен к дополнительному связыванию трехмерной структуры, координируя атомы кислорода амидных групп, что подтверждается снижением относительного объема ПААм-2%-р с ростом концентрации хлорида кальция в растворах. Взаимодействие катиона кальция с функци- ональными группами полиакриламида схематически изображено на рис. 6.
Рис. 6. Взаимодействие катиона кальция с функциональными группами ПААм.
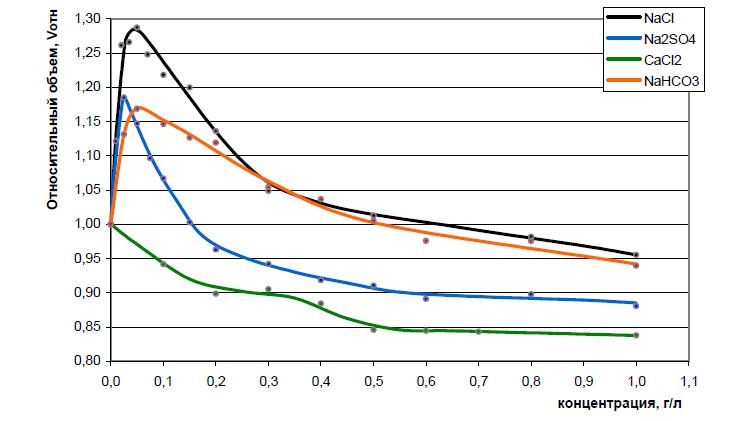
Для наглядности четыре зависимости относительного объема геля ПААм-2%-р от концентрации различных солей нанесены на один график в виде сглаживающих линий (рис. 7).
Рис. 7. Сопоставление влияния концентраций солей в растворах NaCl, Na2SO4, NaHCO3 и CaCl2 на относительный объем геля ПААм 2%-р.
Как видно из приведенных на рис. 7 результатов, ПААм-2%-р оказался гораздо более чувствительным к природе катиона по сравнению с природой аниона, хотя и влияние аниона тоже весьма заметно. В растворах различных натриевых солей зависимости изменения объема от концентрации различны.
Это позволило использовать гидрогель для анализа смешанных растворов.
6. Анализ смесей двух компонентов.
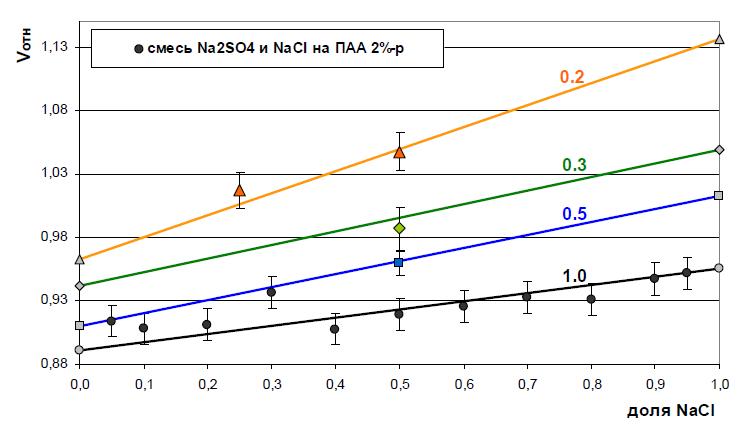
Для наглядного сравнения результатов, полученных при одном соотношении компонентов, но в то же время при разных суммарных концентрациях компонентов в растворах смесей NaCl и Na2SO4, экспериментальные данные нанесены на один рисунок (рис. 8). Во всех случаях наблюдается хорошая корреляция экспериментальных результатов с расчетными значениями.
Рис. 8. Зависимости относительного объема геля ПААм-2%-р, от соотношения компонентов в растворе смеси NaCl и Na2SO4 и от общей концентрации солей в растворе.
Числа над прямыми означают суммарную концентрацию солей, для которой данная прямая является множеством расчетных значений. Экспериментальные значения обозначены точками и окрашены в цвета, соответствующие теоретическим линиям.
Таким образом, полученные результаты подтвердили предположение о том, что относительный объем ПААм-2%-р в растворах смесей, общие концентрации которых не превышают 1 г/л, может быть вычислен по уравнению (6).
7. Анализ смесей трех компонентов.
Следующим шагом, после получения положительных результатов при изучении растворов смесей двух компонентов, стало изучение поведения гидрогелей в растворах смесей трех компонентов, а именно хлорида и сульфата натрия и хлорида кальция. Как видно, в этом случае в анализируемом растворе различалась не только природа катиона, но и природа аниона.
На рис. 9 приведен график, на котором экспериментальные значения относительных объемов геля ПААм-2%-р, полученные для растворов трехкомпонентных смесей разных соотношений, сравниваются с теоретически рассчитанными результатами. Все экспериментально полученные значения относительных объемов и соответствующие им расчетные значения приведены в таблице 3.
Таблица 3. Сравнение экспериментальных и расчетных значений относительных объемов геля ПААм-2%-р в растворах смесей трех компонентов.
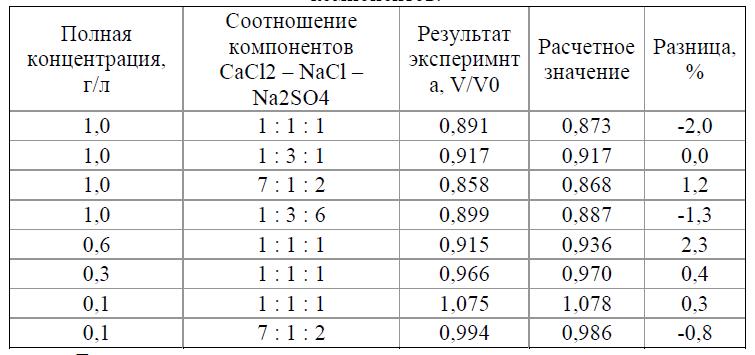 Легко видеть, что расчетные значения для соответствующих экспериментальных результатов попадают в доверительные интервалы этих точек. На данном основании был сделан вывод о том, что ПААм может быть использован для анализа растворов смесей нескольких компонентов.
Легко видеть, что расчетные значения для соответствующих экспериментальных результатов попадают в доверительные интервалы этих точек. На данном основании был сделан вывод о том, что ПААм может быть использован для анализа растворов смесей нескольких компонентов.
На основе проведенных исследований разработана программа «Perebor», позволяющая при помощи нескольких измерений относительного объема геля в растворе рассчитать состав компонентов в смеси. Для определения состава смеси с помощью программы необходимо произвести измерение относительного объема геля в анализируемом растворе, затем произвести разбавление раствора в известное количество раз и снова произвести измерение относительного объема. На основании этих данных можно составить систему уравнений, состоящую из двух уравнений, вида (5) и уравнения связи, основанного на разбавлении в известное количество раз.
Этих уравнений достаточно для определения состава раствора смеси двух компонентов. Для определения трех- и более присутствующих компонентов необходимо произвести дополнительные измерения с другими разбавлениями.
Экспериментальные результаты и погрешности измерений вводятся в программу, указывается путь к массивам данных, полученных для растворов индивидуальных компонентов, после чего программа производит расчет.
Результаты выводятся в виде усредненных (по всем решениям) в рамках доверительных интервалов значений концентраций компонентов в смеси с указанием стандартных отклонений по каждой концентрации.
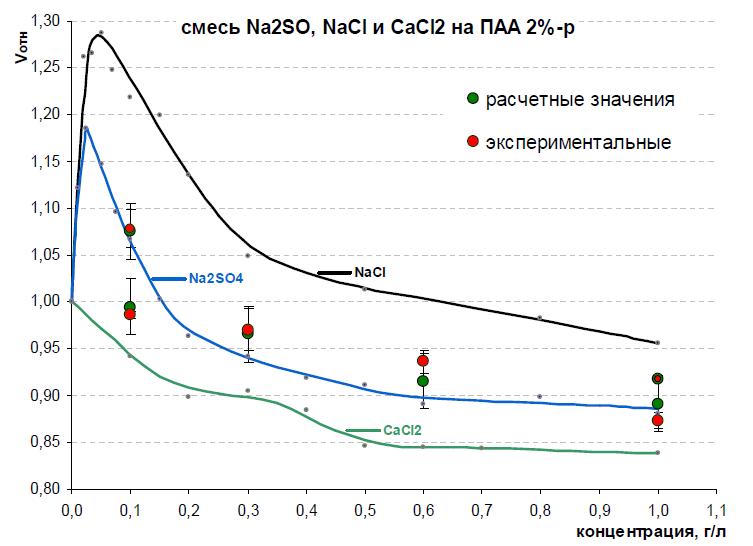 Рис. 9. Сравнение экспериментальных и расчетных значений относительных объемов геля ПААм-2%-р в растворах смесей трех компонентов. Линиями проведены зависимости относительных объемов геля ПААм-2%-р в растворах индивидуальных компонентов, подписанных на графике соответствующими цветами. Красными и зелеными точками соответственно обозначены экспериментальные и расчетные значения для растворов смесей трех компонентов.
Рис. 9. Сравнение экспериментальных и расчетных значений относительных объемов геля ПААм-2%-р в растворах смесей трех компонентов. Линиями проведены зависимости относительных объемов геля ПААм-2%-р в растворах индивидуальных компонентов, подписанных на графике соответствующими цветами. Красными и зелеными точками соответственно обозначены экспериментальные и расчетные значения для растворов смесей трех компонентов.
ЛИТЕРАТУРА.
- Фриман Д.Х. Изучение ионообменных систем с помощью микроскопа. /В кн.: Ионный обмен (Под ред. Я. Маринского). М.: Мир. 1968. С. 332-367 40.Ковалева С.С., Ферапонтов Н.Б. Влияние природы растворенного вещества на набухание геля поливинилового спирта// Сорбционн. и хроматогр. процессы. 2007. Т.7 Вып.6. С. 883-894.
- Кавалерская Н.В., Ферапонтов Н.Б. Поведение сшитого полиакриламида в растворах низкомолекулярных электролитов. // Сорб. и хром. процессы 2009. T. 9. Вып. 3. С. 433-440.
- Ферапонтов Н.Б., Рубин Ф.Ф., Ковалева С.С. Безреагентный способ определения содержания компонентов в растворе и устройство для его осуществления.// Патент РФ № 228250 от 29 апреля 2005 г. БИ № 24 от 27 августа 2006 г. (Заявка № 2005112942/04(014936) от 29 апреля 2005 г.).
- Ферапонтов Н.Б., Ковалева С.С., Рубин Ф.Ф. Определение природы и концентрации растворенных веществ методом набухающей гранулы// Журн. аналит. химии. 2007. Т.62, №10, с.1028-1033.
- Кудухова И.Г., Рудаков О.Б., Рудакова Л.В., Ферапонтов Н.Б. Кинетика набухания гранул из ионогенных и неионогенных полимерных материалов в водно-спиртовых растворах // Сорбционные и хроматографические процессы. 2010. Т. 10. Вып. 4. С. 589-594.
- Кудухова И.Г., Рудаков О.Б., Рудакова Л.В., Ферапонтов Н.Б. Новый способ контроля содержания воды в водно-спиртовых смесях, основанный на микрофотографическом измерении эффектов набухания полимерных гранул // Сорбционные и хроматографические процессы. 2010. Т. 10. Вып. 5. С. 759-761.
- Цундель Г. Гидратация и межмолекулярное взаимодействие. Исследование полиэлектролитов методом инфракрасной спектроскопии. М.: Мир. 1972. 404с.
- Aquilanti V., Cappelletti D., Pirani F. Range and strength of interatomic forces: dispersion and induction contributions to he bonds of dications and of ionic molecules.// Сhemical Physics. 1996. V. 209. p.299-311.