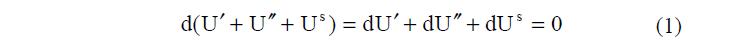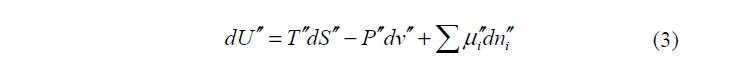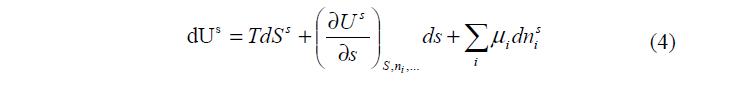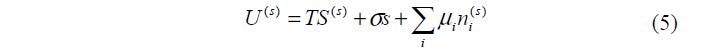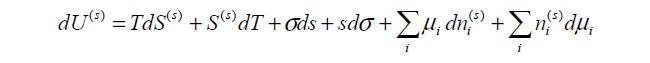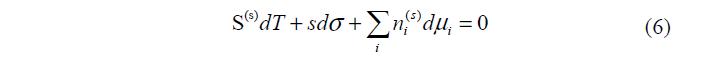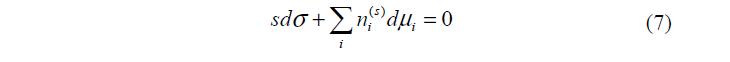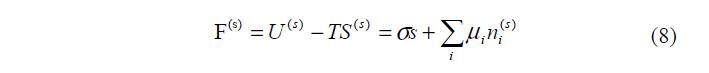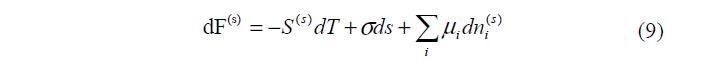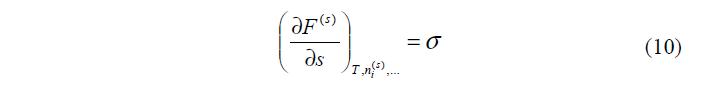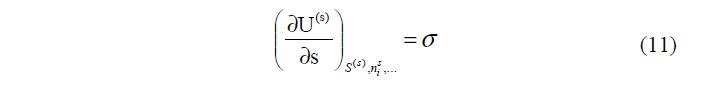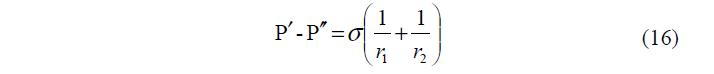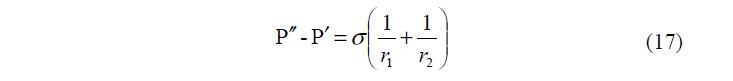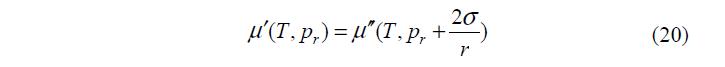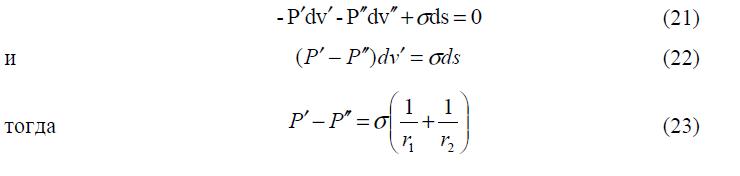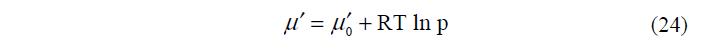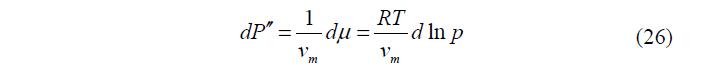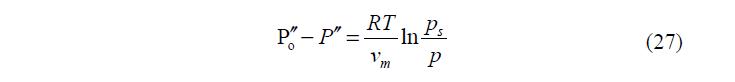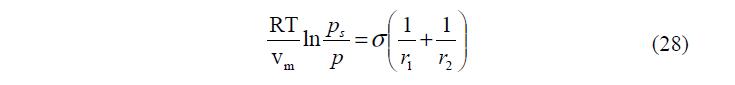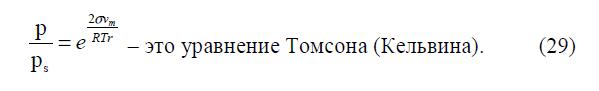Физическая химия полимерных гелей Лекция 10 ПАРАДОКС ШРЕДЕРА. ПРИЧИНЫ РАЗЛИЧНОГО НАБУХАНИЯ ПОЛИМЕРОВ В ПАРЕ И В ЖИДКОСТИ

Физическая химия полимерных гелей Лекция 9 ВЛИЯНИЕ ПОЛИМЕРНОЙ МАТРИЦЫ НА АКТИВНОСТЬ ВОДЫ В ГИДРОФИЛЬНЫХ ПОЛИМЕРАХ. КОНСТАНТА РАСПРЕДЕЛЕНИЯ ВОДЫ
09.12.2015
Физическая химия полимерных гелей Лекция 11 ПОЛИМЕРНЫЙ РАСТВОР, ЭТО ПОВЕРХНОСТНЫЙ СЛОЙ?
18.12.2015Физическая химия полимерных гелей Лекция 10 ПАРАДОКС ШРЕДЕРА. ПРИЧИНЫ РАЗЛИЧНОГО НАБУХАНИЯ ПОЛИМЕРОВ В ПАРЕ И В ЖИДКОСТИ
Физическая химия полимерных гелей
Ферапонтов Н. Б., Гагарин А. Н., Струсовская Н. Л., Токмачёв М. Г.
Москва, МГУ имени М. В. Ломоносова 2015 г.
Известно, что при помещении полимера в атмосферу водяного пара, его масса и объем увеличиваются в соответствии с количеством сорбированной воды, которое описывается изотермой сорбции. Однако, если набухший в паре полимер поместить в воду, то его объем увеличится еще больше. Пример, подтверждающий этот факт, носит название эффекта Шредера [1]. Его суть проиллюстрирована на рис.1. Хорошо видно, что при одинаковой активности воды, степень набухания полоски полимера зависит от того в жидкой или паровой фазе она находится.
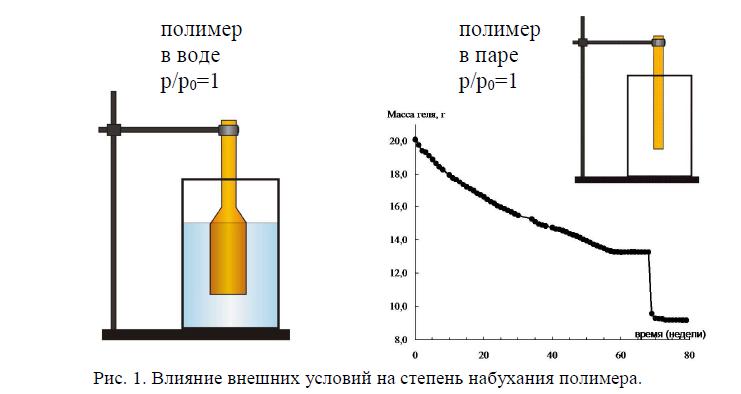
Рис. 1. Влияние внешних условий на степень набухания полимера.
При помещении полимера в жидкость, ее проникновение внутрь приводит к заметному увеличению его объема, однако, если полимер снова перенести в атмосферу пара, то, как показано на графике, масса полимера, медленно уменьшаясь, достигнет значений, соответствующих массе полимера в паре. Испарение воды из набухшего полимера носит общий характер и называется «синерезис». Если затем поместить полимер в эксикатор с Р2О5, то его масса снизится еще больше и достигнет массы сухого полимера (см.
график на рис.1).
полимер в воде p/p0=1 полимер в паре p/p0=1 Чтобы понять и количественно описать набухание полимера при его переносе из одной фазы в другую, надо разобраться в причинах и механизмах взаимодействия полимера с растворителем, находящимся в разных фазовых состояниях.
1. Условия равновесия в гетерофазных системах. Поверхностный слой и его свойства.
Общим условием равновесия любой замкнутой системы при постоянных значениях общей энтропии, общего объема и общего количества каждого из компонентов является минимум ее внутренней энергии [2]. Если при равновесии в изолированной системе две фазы соприкасаются друг с другом, то между ними существует поверхность раздела. Так как эта поверхность имеет реальную толщину, то ее называют поверхностным слоем. Изменение поля молекулярных сил, происходящее в этом слое между фазами 1 и 2 , приводит к отличию величин энергии Us, энтропии Ss и чисел молей компонентов этого слоя ns от соответствующих величин в контактирующих фазах. Поэтому для равновесия системы, состоящей из двух объемных фаз 1 и 2 и поверхностного слоя между ними, должно соблюдаться условие:
где dUs – изменение внутренней энергии поверхностного слоя между фазами.
Состав поверхностного слоя зависит от природы и доли каждого из компонентов в контактирующих фазах. Кроме этого, на свойства веществ, находящихся в объеме слоя оказывает влияние форма поверхности раздела.
Так как энергия поверхностного слоя линейно связана с площадью поверхности раздела, то вклад этого члена особенно заметен в системах, обладающих развитыми поверхностями такими, например, как дисперсные и пористые среды. Изменения внутренних энергий соприкасающихся с поверхностным слоем фаз 1 и 2 будут:
Изменение внутренней энергии поверхностного слоя происходит в результате изменения величины и (или) положения поверхности раздела, так что:
где величина s = ? ? ? ? ? ? ? ? ¶ ¶ , ,…
s ( ) ( ) s U s i S s n . Ее называют поверхностным натяжением слоя. Размерность поверхностного натяжения s : эрг/см2 или дин/см.
Величины поверхностной энтропии S(s) и адсорбции, точнее количеств компонентов в поверхностном слое (s) i n пропорциональны поверхности раздела s. Поэтому величина U(s) пропорциональна этим факторам емкости, то есть согласно уравнению (4)
Полный дифференциал величины U ( s) имеет вид:
Это выражение совместно с (4) лишь при условии следующей связи между изменениями факторов интенсивности в поверхностном слое:
Отсюда при постоянной температуре получается
Это фундаментальные уравнения Гиббса для межфазного поверхностного слоя. Уравнение (7) аналогично уравнению Гиббса–Дюгема для объемной фазы.
Определим избыточную свободную энергию поверхностного слоя.
Выражение для свободной энергии F=U?TS. В соответствии с уравнением (5)
Из этого определения и из уравнения (6) следует, что
Это уравнение позволяет определить межфазное поверхностное натяжение как свободную поверхностную энергию единицы поверхности при постоянной температуре и постоянном составе слоя
То есть величину ? можно рассматривать как свободную энергию едини- цы поверхности. Напомним, что эту же величину называют поверхностным натяжением слоя.
Изменение или смещение поверхности s, кроме изменения внутренней энергии слоя, вызывает изменение объема контактирующих фаз 1 и 2 на вели- чины dv? и dv??, причем из условия постоянства объема всей системы следует:
Очевидно (см. уравнения 2 и 3), что эти изменения объемов вызовут дополнительные изменения внутренних энергий в фазах 1 и 2 на величины
При равновесии общее изменение энергии системы, связанное со смещением поверхности s, равно нолю, поэтому условие механического равновесия системы, состоящей из двух фаз (1 и 2) и поверхностного слоя между ними, будет следующее
Это условие механического равновесия отличается от условия равенства давлений в объемных фазах. Действительно из (14) и условия постоянства объемов (12) следует, что
Выражение (15) показывает, что при изменении поверхности раздела s гидростатические давления в объемных фазах изменяются по-разному. То есть возникает некоторое различие во внешних давлениях на каждую из фаз, которое обычно компенсируется высотой столба жидкости.
Так как изменения объема dv и поверхности ds не являются независимыми, то в результате анализа уравнений, связывающих изменение площади поверхности с ее кривизной (радиусами) из уравнения (15) можно получить равенство:
где 1 2 r , r – радиусы кривизны поверхности s. Причем центры кривизны лежат в фазе 1. Если центры кривизны лежат в фазе 2, то
Из уравнений (16 и 17) следует, что разность гидростатических давлений в смежных фазах равна произведению межфазного поверхностного натяжения на кривизну поверхности. Это основные уравнения механического равновесия для поверхностей раздела: жидкость-пар. Давления P?, P?? равны только в том случае, когда r1=r2=0, то есть когда поверхность раздела плоская.
Если поверхность раздела не является плоской, и существует некоторый эффект, обусловленный поверхностным натяжением, то в контактирующих фазах давление будет различным, то есть P? ? P??. Тем не менее, при равновесии должно соблюдаться равенство:
2. Влияние поверхностного натяжения на границе гидратированный полимер – водяной пар. Капиллярная конденсация. Уравнение Кельвина.
Капиллярная конденсация, это сжижение пара в капиллярах, щелях или порах в твердых телах. Мы уже говорили о том, что в состоянии термодинамического равновесия каждый из компонентов характеризуется одним и тем же химическим потенциалом во всем объеме исследуемой системы. То есть химический потенциал любого из компонентов одинаков во всех фазах, где он присутствует, а условия равновесия для энергии переноса массы определяются соотношением:
Если химические потенциалы компонента в двух контактирующих фазах не равны, то этот компонент будет перемещаться из фазы с большим химическим потенциалом в фазу с меньшим химическим потенциалом. Если такой перенос невозможен, то выравнивание значений химических потенциалов между фазами происходит в результате образования перепада давлений. Выравнивание значений химических потенциалов за счет разницы в фазовых давлениях наблюдается, например, в результате искривления поверхности раздела (капиллярные явления) ( рис. 2). В этом случае в качестве «компенсатора давления» выступает поверхностное натяжение. Из уравнений (16,17 и 19) следует, что радиус r сферической капли жидкости и давление ее паров (рис.3) связаны условием:
где: pr – давление пара, находящегося в равновесии с каплей, радиусом r, то есть давление насыщенного пара жидкой капли; m ? – химический потенциал вещества в паре; m ?? – химический потенциал вещества в жидкости. Из него видно, что из-за поверхностного натяжения давление насыщенного пара рr над жидкой каплей радиусом r больше, чем давление ps над плоской поверхностью жидкости.
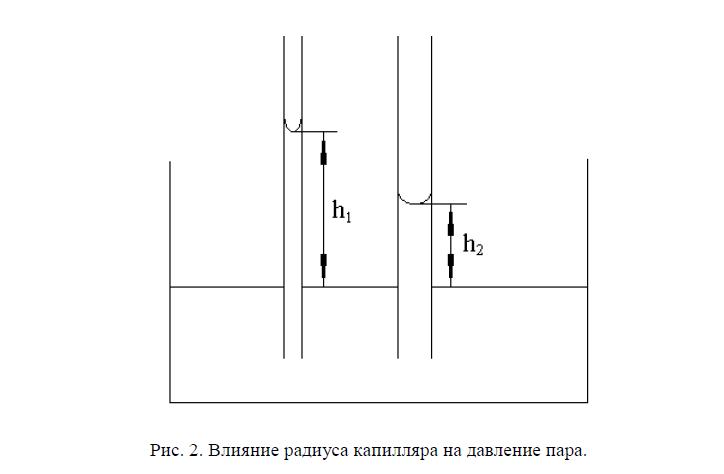
Рис. 2. Влияние радиуса капилляра на давление пара.
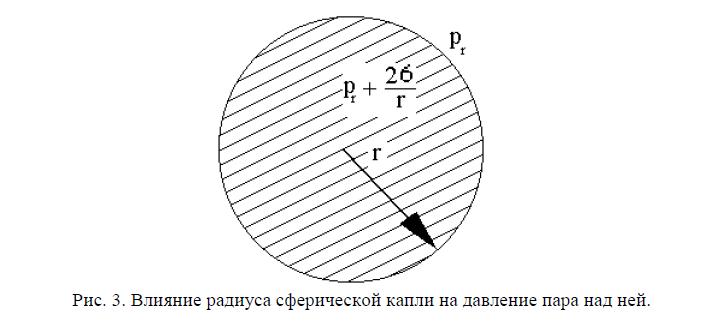
Рис. 3. Влияние радиуса сферической капли на давление пара над ней.
Конденсация пара в порах адсорбента связана как с давлением пара, так и с радиусом капилляра (кривизной поверхности). В случае конденсации пара и образования искривленной поверхности жидкость-пар, условия равновесия такой системы выражаются уравнениями
Давление пара над поверхностью жидкости определяется величиной химического потенциала пара:
Так как при равновесии пара с жидкостью химические потенциалы компонента в фазах равны, то можно записать, что
С другой стороны, известно, что m T v = ? ? ? ?? ? ¶ ?? ¶ ?? P m , где vm– мольный объем жидкости. Следовательно, уравнение (25) можно переписать в виде:
Интегрируя от давления P?? , соответствующего данной кривизне поверхности и давлению пара p, до давления о P?? , соответствующего плоской поверхности и давлению насыщенного пара над плоской поверхностью ps, находим, считая vm постоянным:
Так как для плоской поверхности о ?? = P? о P , а общее давление в газовой фазе (пар+газ) не изменяется, то есть ? = P? о P , то из уравнений (16 и 27) получаем:
Для выпуклого шаровидного мениска уравнение (28) принимает вид:
Из него следует, что с ростом кривизны выпуклой поверхности жидкости давление пара над ней увеличивается. Следовательно, над выпуклыми менисками равновесное давление пара будет больше, чем над плоской поверхностью. Если в исследуемой системе есть две поверхности: выпуклая и гладкая, то возникнет поток через фазу пара от выпуклой поверхности к гладкой. Поверхность ПГ состоит из гидратированных полимерных цепей, являющихся частью полимерного каркаса геля. Промежутки между цепями заполнены “свободной” водой или раствором. При переносе ПГ из жидкости в атмосферу пара на поверхности раздела ПГ – пар возникает поверхностное натяжение, под действием которого, “свободная” вода на поверхности ПГ, образует выпуклые мениски. Давление пара над такими менисками больше давления пара в остальном объеме системы, что и является причиной испарения воды из ПГ, т.е. явления синерезиса. Отметим, что подобным образом из ПГ испаряется только “свободная” вода. “Связанная” вода, т.е.
вода, сорбированная полимером, остается в полимере.
Таким образом причиной «эффекта Шредера» является гетерофазность ПГ, в котором одновременно присутствуют два вида воды с разными свойствами.
«Свободная» вода (или раствор) проникает в полимер только в результа- те помещения полимера в жидкость. В жидкости исчезает поверхностное натяжение, существовавшее на границе полимер – пар, что приводит к самопроизвольному растворению гидратированных полимерных цепей.
ЛИТЕРАТУРА
1. Schroeder P. Ueber Erstarrungs- und Quellungserscheinungen von Gelatine.//Z.Phys. Chem. 1903. Bd.45. S.75-117./
2. Герасимов Я.И. Курс физической химии// М.: Химия, 1971. 592 с.