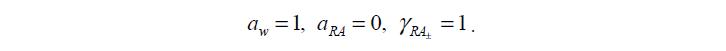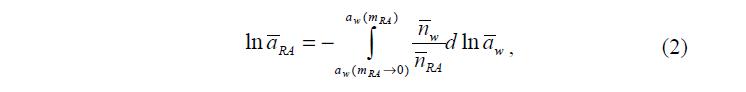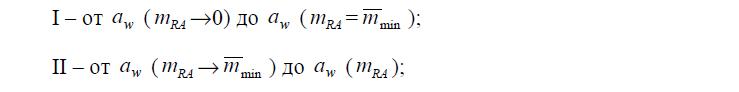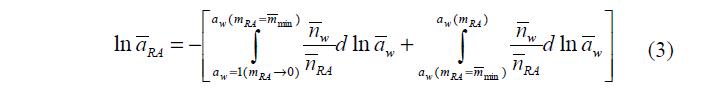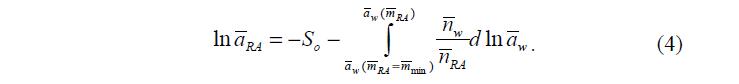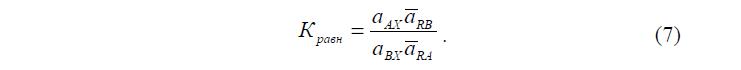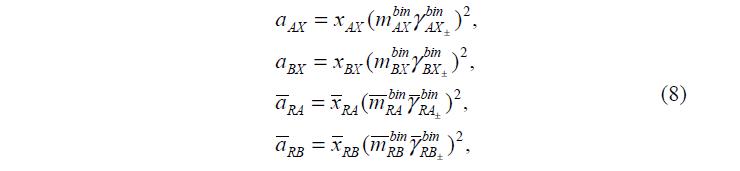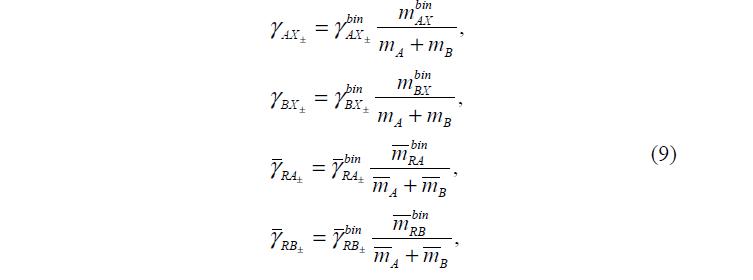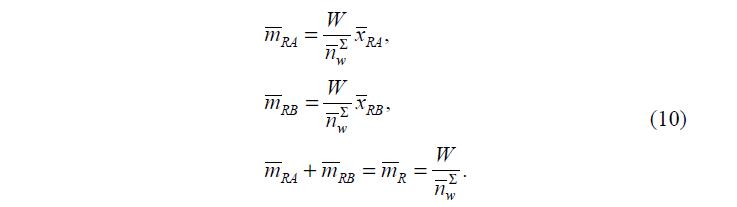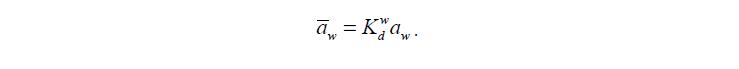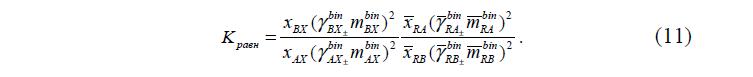Физическая химия полимерных гелей Лекция 14 АКТИВНОСТИ ПОЛЯРНЫХ ГРУПП В ПОЛИМЕРНОМ РАСТВОРЕ

Физическая химия полимерных гелей Лекция 13 НЕКОВАЛЕНТНЫЕ СШИВКИ В ПОЛИМЕРНЫХ ГЕЛЯХ.
18.12.2015
Физическая химия полимерных гелей Лекция 15 ВЗАИМОДЕЙСТВИЕ РАСТВОРЕННЫХ ВЕЩЕСТВ С ПОЛЯРНЫМИ ГРУППАМИ. КОНСТАНТЫ РАСПРЕДЕЛЕНИЯ РАСТВОРЕННЫХ ВЕЩЕСТВ В ПОЛИМЕРНЫХ ГЕЛЯХ.
19.12.2015Физическая химия полимерных гелей Лекция 14 АКТИВНОСТИ ПОЛЯРНЫХ ГРУПП В ПОЛИМЕРНОМ РАСТВОРЕ
Физическая химия полимерных гелей
Ферапонтов Н. Б., Гагарин А. Н., Струсовская Н. Л., Токмачёв М. Г.
Москва, МГУ имени М. В. Ломоносова 2015 г.
1. Определение активности полярной группы в бинарном полимерном растворе.
Запишем уравнение Гиббса–Дюгема для моноионной формы ПР:
Здесь w n и RA n – числа молей компонентов ПР, а w m и AR m – их химические потенциалы. Для удобства примем = 1 RA n .
В качестве отсчетного состояния для ПР выбираем бесконечно разбавленный раствор мономера соответствующей природы. В нем
где RA RA m = m – моляльности ПР.
При равновесии с водой ПР имеет минимальную моляльную концентрацию min m . Поэтому весь интервал интегрирования (от = 1 w a при ®0 RA m до w a при mRA) целесообразно разбить на два участка:
Тогда уравнение (2) может быть записано как:
В качестве исходных для проведения интегрирования воспользуемся справочными данными зависимости nw = f( w a ) для мономера (см. лекцию 8).
Так как количество поперечных связей в конкретном полимере есть величина постоянная, то первый член уравнения (3) для этого случая тоже является константой. Обозначим его So. Тогда уравнение (3) превращается в:
Из сказанного следует, что для расчета активности полярной группы в бинарном ПР необходимо знать зависимость nw = f( w a ) для раствора мономера соответствующей природы, w d K и активность воды во внешнем равновесном растворе [1].
2. Определение состава и свойств полимерного раствора, находящегося в смешанной ионной форме.
Если ПР обработать раствором, содержащим электролиты АХ и ВХ, где А и В – ионы того же знака, что и противоион в ПР, то в результате будет получена так называемая смешанная ионная форма ПР. Если электролиты АХ и ВХ не проникают в фазу ПР, равновесие между фазами будет представлять собой равновесие между раствором, содержащим электролиты АХ и ВХ, и ПР в смешанной RA– и RB–формах – обычное ионообменное равновесие (рис. 1).
С позиций двухфазной модели набухшая смешанная ионная форма должна рассматриваться как раствор, состоящий из двух полиэлектролитов RA и RB, а также воды. Доли каждого из полиэлектролитов RA и RB могут быть различными, но сумма этих долей равна единице (уравнение 5).
Суммарное количество воды в ПР определяют с помощью уравнения (6):
 Рис. 1. Составы и характеристики компонентов фаз при равновесиимежду смешанным раствором НМЭ и смешанной ионной формой ПР.
Рис. 1. Составы и характеристики компонентов фаз при равновесиимежду смешанным раствором НМЭ и смешанной ионной формой ПР.
Так как суммарное количество воды S w n в ПР зависит от доли каждой из ионных форм, то в соответствии с этим будут меняться и концентрация ПР и все связанные с ней параметры. Для описания равновесия в таких системах воспользуемся законом действия масс. В этом случае для 1–1 электролитов и случаев, когда заряд ионообменной группы равен единице
Если, провести эксперимент и установить мольные доли каждой из ионных форм, то определение численного значения константы ионообменного равновесия будет выглядеть следующим образом. Сначала, воспользовавшись результатами работ А. Б. Здановского [2] и Г. И. Микулина [3], записывают выражения для активностей и коэффициентов активностей каждого из компонентов, входящих в уравнение (7):
где bin RB bin RA bin BХ bin AХ m ,m ,m ,m – моляльные концентрации каждого из указанных электролитов в их бинарных растворах при активности воды, равной активности воды в исследуемой смеси ( bin aw = аw S ); AX BX RA RB x , x , x , x – их доли в соответствующих растворах.
Средние моляльные коэффициенты активности ( AХ ± g , XB± g и RA± g , RB± g ) вычисляют по уравнениям (9):
где A B X A B R m ,m ,m ,m ,m ,m – моляльные концентрации соответствующих ионов в соответствующих фазах; bin RB bin RA bin BX bin AX± ± ± ± g ,g ,g ,g – табличные величины, соответствующие средним моляльным коэффициентам активности электролитов в бинарных растворах с активностью воды, соответствующей активности воды в смеси [4].
Определить моляльные концентрации (mAX, mBX, mX) каждого их компонентов раствора НМЭ не представляет труда. Моляльные концентрации компонентов в фазе ПР вычисляют по уравнениям (10): .
Для нахождения bin RA± g и bin RB± g надо знать активность воды в фазе ПР ( w a ). Эту величину находят, воспользовавшись константой распределения воды ( w d K ):
После того, как все члены системы (8) найдены, выражение для Кравн примет вид:
В отличие от константы распределения ( d K ) для константы равновесия (Кравн) нельзя сделать однозначного вывода о влиянии на нее количества сшивающего агента (поперечных связей). Однако, принимая во внимание, что при изменении w a (а это функция количества сшивающего агента) изменение моляльностей (m ) и средних моляльных коэффициентов активностей ( bin ± g ) для различных НМС не одинаковые, можно предположить, что изменение количества поперечных связей приводит к изменению численного значения константы ионообменного равновесия (Кравн).
ЛИТЕРАТУРА
1. Ferapontov N. B., Parbuzina L. R., Gorshkov V. I., Strusovskaya N. L., Gagarin A. N. Interaction of cross-linked polyelectrolytes with solutions of low-molecularweight electrolytes. // Reactive & Functional Polymers. 2000. V.45. p. 145–153.
2. Здановский А.Б. Закономерности в изменении свойств смешанных растворов.// Тр. соляной лаборатории АН СССР. 1936. Вып.6. 70с.
3. Микулин Г.И., Вознесенская И.Е. Теория смешанных растворов электролитов, подчиняющихся правилу Здановского. Часть I. Растворы двух солей с общим ионом.// Вопросы физической химии растворов электролитов: Сб. статей/ Под ред. Г.И. Микулина. Л.: Химия 1968. С.304-329.
4. Kenneth S. Pitter Thermodytriarnics of Electrolytes. I . Theoretical Basis and General Equation // The Journal of Physical Chemistry, 1973, Vol. 77, No. 2, p. 268-277